resultados de la búsqueda: profesionales/aviso-importante/wp-content/uploads/logos/Sitio web no disponible/inicio/Sitio web no disponible
Aviso Legal
0. RECOMENDACIÓN PREVIA:
Por favor, lea todos los apartados del presente aviso legal y nuestra política de privacidad antes de utilizar este website. Las siguientes condiciones son vinculantes para cualquier usuario del mismo. Documento revisado el 28/06/2021.
En cumplimiento con el deber de información dispuesto en la Ley 34/2002 de Servicios de la Sociedad de la Información y el Comercio Electrónico (LSSI-CE) de 11 de julio, se facilitan a continuación los siguientes datos de información general de este sitio web.
La razón de este texto es explicarle de manera detallada las funcionalidades de esta web y aportarle toda la información relacionada con el responsable y la finalidad de los contenidos incluidos en ella.
1. INTRODUCCIÓN; DATOS IDENTIFICATIVOS y USUARIOS:
El presente aviso legal y política de privacidad regula el uso del servicio del PORTAL de Internet www.seaic.org informándole en cumplimiento de la Ley 34/2002, de 11 de julio lo siguiente:
- Titular: SOCIEDAD ESPAÑOLA DE ALERGOLOGIA E INMUNOLOGIA CLINICA (SEAIC). CIF/NIF: G-58318395
- Domicilio social: Calle Agustín de Foxá 25, 28036 Madrid
- Inscrita en el Registro en el Registro Nacional de Asociaciones, Sección 1, Número Nacional 3446.
- Correo electrónico: seaic@seaic.org Teléfono: 915 348 826
- Actividad social: Sociedad profesional y científica, sin ánimo de lucro, que desarrolla sus actividades en todo el territorio del Estado español y está constituida por profesionales que trabajan en el estudio de las enfermedades de mecanismo inmunológico, particularmente por hipersensibilidad.
- Finalidad de la página web: Dar a conocer sus actividades, contactar, suscripciones y realizar alta de asociados.
El presente documento tiene por objeto establecer los términos y condiciones generales de uso del PORTAL. Los términos y condiciones generales son de obligada aceptación y cumplimiento por parte de todos las personas, profesionales y empresas (en adelante el USUARIO), que deseen hacer uso de los mismos (actuales o nuevos servicios que SEAIC preste en el futuro a través del PORTAL).
2. OBLIGACIONES DE LOS USUARIOS, USO DEL SITIO WEB, SUS SERVICIOS Y CONTENIDOS;
El usuario se compromete a utilizar el portal, el contenido y servicios, sin contravenir la legislación vigente, los usos generalmente aceptados y el orden público. Queda prohibido, el uso del Web con fines ilícitos o lesivos contra SEAIC o un tercero, que, de cualquier forma, puedan causar perjuicio o impedir el normal uso del PORTAL.
SEAIC garantiza que los contenidos y servicios que ofrece el portal respetan el principio de dignidad de la persona, de protección de la juventud y la infancia, de no-discriminación por motivos de raza, sexo, religión, opinión, nacionalidad, discapacidad o cualquier otro aspecto personal y social. SEAIC se reserva el derecho de retirar todos aquellos comentarios y aportaciones que vulneren la ley o no respeten los principios señalados.
SEAIC es titular o se encuentra debidamente autorizada para su difusión por sus legítimos titulares, de los derechos de propiedad intelectual e industrial sobre las marcas, imágenes, textos, diseños, animaciones, o cualquier otro contenido o elementos de este portal. Cualquier acto de reproducción, distribución, comunicación pública, puesta a disposición, o transformación, así como cualquier otra forma de explotación de todo o parte de dichos contenidos o elementos, realizado bajo cualquier forma o mediante cualquier medio, requerirá el consentimiento previo y por escrito de SEAIC.
Las presentes Condiciones Generales de Uso del PORTAL no confieren al USUARIO ningún otro derecho de uso, alteración, explotación, reproducción, distribución o comunicación pública del Portal y/o de sus Contenidos distintos de los aquí expresamente previstos. Los contenidos (información, archivos de sonido y/o imagen, fotografías, diseños, etc.) recogidos en el portal, son propiedad de SEAIC o se encuentra debidamente autorizada para su difusión por sus legítimos titulares. SEAIC se compromete a no realizar publicidad engañosa y por tanto, queda prohibido:
- El uso para todo tipo de fines comerciales o publicitarios, distintos de los estrictamente permitidos.
- Su reproducción, publicación, distribución o modificación, total o parcial a menos que se cuente con la autorización previa y por escrito de sus legítimos titulares o resulte legalmente permitido.
- Cualquier vulneración de los derechos de SEAIC o de sus legítimos titulares sobre los mismos.
3. PROPIEDAD INTELECTUAL E INDUSTRIAL;
En todo caso, el USUARIO reconoce y acepta que todos los derechos de propiedad industrial e intelectual sobre los Contenidos y/o cualesquiera otros elementos insertados en el portal pertenecen a SEAIC o se encuentra debidamente autorizada para su difusión en el presente PORTAL. En el caso de que un usuario o un tercero consideren que se ha producido una violación de sus legítimos derechos de propiedad intelectual por la introducción de un determinado contenido en el Web, deberá notificar dicha circunstancia a SEAIC indicado:
- Datos personales del interesado titular de los derechos presuntamente infringidos, o indicar la representación con la que actúa en caso de que la reclamación la presente un tercero distinto del interesado.
- Señalar los contenidos protegidos por los derechos de propiedad intelectual y su ubicación en el Web, la acreditación de los derechos de propiedad intelectual señalados y declaración expresa en la que el interesado se responsabiliza de la veracidad de las informaciones facilitadas en la notificación.
4. ENLACES
El PORTAL proporciona enlaces a otros sitios web propios y contenidos que son propiedad de terceros. El único objeto de los enlaces es proporcionar al usuario la posibilidad de acceder a dichos enlaces. SEAIC no se responsabiliza en ningún caso de los resultados que puedan derivarse al usuario por acceso a dichos enlaces.
El usuario que se proponga establecer cualquier dispositivo técnico de enlace desde su sitio web al portal www.seaic.org deberá obtener la autorización previa y escrita de SEAIC. El establecimiento del enlace no implica en ningún caso la existencia de relaciones entre el PORTAL y el propietario del sitio en el que se establezca el enlace, ni la aceptación o aprobación por parte de www.seaic.org de sus contenidos o servicios.
5. MODIFICACIÓN UNILATERAL Y DURACIÓN;
SEAIC se reserva el derecho de modificar, en cualquier momento y sin necesidad de previo aviso, la presentación y configuración del PORTAL web www.seaic.org como el presente aviso legal.
6. EXCLUSIÓN DE GARANTÍAS Y RESPONSABILIDAD;
SEAIC no otorga ninguna garantía ni se hace responsable, en ningún caso, de los daños y perjuicios de cualquier naturaleza que pudieran acarrear a causa de:
- La falta disponibilidad, mantenimiento y efectivo funcionamiento del Web y/o de sus servicios o contenidos.
- La existencia de virus, programas maliciosos o lesivos en los contenidos.
- El uso ilícito, negligente, fraudulento, contrario a las presentes Condiciones Generales, a la buena fe, a los usos generalmente aceptados o al orden público, del sitio Web, sus servicios o contenidos, por parte de los usuarios.
7. TRATAMIENTO DE DATOS PERSONALES
SEAIC, tal y como recoge en su “POLITICA DE PRIVACIDAD” que puede consultar en nuestra web, ha adoptado los niveles de seguridad adecuados a los datos que trata y gestiona, incorporando todos los medios y medidas técnicas a su alcance para garantizar su confidencialidad, evitar su mal uso, pérdida, alteración, acceso no autorizado y robo.
8. LEGISLACIÓN APLICABLE Y JURISDICCIÓN;
Las presentes Condiciones Generales se regirán por la legislación española, sometidas a los juzgados y tribunales de la ciudad de Madrid (España) ante cualquier controversia derivada del acceso al PORTAL.
9. CONTACTO
En caso de que cualquier Usuario tuviese alguna duda acerca de este aviso legal o cualquier comentario sobre la web puede dirigirse a seaic@seaic.org
Concurso de logos 70/40
Con motivo de la conmemoración de los 70 años de nuestra sociedad y los 40 años del reconocimiento de nuestra especialidad, se ha convocado un concurso de logos para ser utilizados durante todo el año. Hasta el día 31 de marzo, todos los socios pueden votar sus opciones preferidas.
Aviso importante
Área de formación continuada del JIACI
Estimados socios:
El registro de alta para participar en la página de evaluación del Journal of Investigational Allergology and Clinical Immunology se realizará personalmente mediante solicitud enviada por correo electrónico dirigido al webmaster (webmaster@seaic.org). Para ello pueden utilizar el formulario que a tal efecto existe en el área de contacto, especificando nombre, apellidos y localidad de trabajo.
Si ya existe un registro previo, basta con acceder directamente con las credenciales y seleccionar el examen. En caso de cualquier problema de acceso, también se puede notificar por correo electrónico a la misma dirección.
Es importante recordar a los participantes que la respuesta a su solicitud se puede demorar unos días, por lo que no es recomendable contactar poco antes de finalizar el plazo de un examen. Por otra parte, rogamos a los socios registrados que guarden sus credenciales para futuras evaluaciones.
Política de Cookies
La presente política de cookies ha sido actualizada por última vez el 09/05/2025.
En esta web, de la que es titular la SOCIEDAD ESPAÑOLA DE ALERGOLOGÍA E INMUNOLOGÍA CLÍNICA, recopilamos y utilizamos la información según indicamos en nuestra política de privacidad. Una de las formas en las que recopilamos información es a través del uso de la tecnología llamada “cookies”. Desde la web de SOCIEDAD ESPAÑOLA DE ALERGOLOGÍA E INMUNOLOGÍA CLÍNICA, www.seaic.org, utilizamos cookies para varias cosas.
En todo caso, tiene más información y en detalle en “Guía sobre el uso de las cookies” de la AEPD y en su página web https://www.aepd.es/es
Tipos de cookies utilizadas
Este Web utiliza tanto cookies temporales de sesión como cookies permanentes. Las cookies de sesión almacenan datos únicamente mientras el usuario accede al Web y las cookies permanentes almacenan los datos en el terminal para que sean accedidos y utilizados en más de una sesión.
¿Qué es una cookie?
Una “cookie” es una pequeña cantidad de texto que se almacena en tu navegador (como Chrome de Google o Safari de Apple) cuando navegas por la mayoría de los sitios web.
¿Qué NO es una cookie?
No es un virus, ni un troyano, ni un gusano, ni spam, ni spyware, ni abre ventanas pop-up.
¿Qué información almacena una cookie?
Las cookies no suelen almacenar información sensible sobre usted, como tarjetas de crédito o datos bancarios, fotografías o información personal, etc. Los datos que guardan son de carácter técnico, estadísticos, preferencias personales, personalización de contenidos, etc.
El servidor web no le asocia a usted como persona sino a su navegador web. De hecho, si usted navega habitualmente con el navegador Chrome y prueba a navegar por la misma web con el navegador Firefox, verá que la web no se da cuenta que es usted la misma persona porque en realidad está asociando la información al navegador, no a la persona.
¿Qué tipo de cookies existen?
- Cookies técnicas: Son las más elementales y permiten, entre otras cosas, saber cuándo está navegando un humano o una aplicación automatizada, cuándo navega un usuario anónimo y uno registrado, tareas básicas para el funcionamiento de cualquier web dinámica. Por ejemplo, controlar el tráfico y la comunicación de datos, identificar la sesión, acceder a las partes Web de acceso restringido, recordar los elementos que integran un pedido, realizar la solicitud de inscripción o participación en un evento, utilizar elementos de seguridad durante la navegación y almacenar contenidos para la difusión de videos o sonido.
- Cookies de análisis: Recogen información sobre el tipo de navegación que está realizando, las secciones que más utiliza, productos consultados, franja horaria de uso, idioma, etc. Permiten al responsable de las mismas, el seguimiento y análisis del comportamiento de los usuarios de los sitios web a los que están vinculadas
- Cookies de personalización: Son aquéllas que permiten al usuario acceder al servicio con algunas características de carácter general predefinidas en su terminal o que el propio usuario defina. Por ejemplo, el idioma, el tipo de navegador a través del cual accede al servicio, el diseño de contenidos seleccionado, geolocalización del terminal y la configuración regional desde donde se accede al servicio.
- Cookies publicitarias: Muestran publicidad en función de su navegación, su país de procedencia, idioma, etc.
- Cookies de publicidad comportamental: almacenan información del comportamiento de los usuarios obtenida a través de la observación continuada de sus hábitos de navegación, lo que permite desarrollar un perfil específico para mostrar publicidad en función del mismo.
¿Qué son las cookies propias y las de terceros?
Las cookies propias son las generadas por la página que está visitando y las de terceros son las generadas por servicios o proveedores externos como Google, Mailchimp, Mailrelay, LinkedIn, Facebook, Twitter, Google adsense, etc.
¿Qué cookies utiliza esta web?
Esta web utiliza cookies propias y de terceros para analizar el tráfico de nuestra web y de acceso a las redes sociales en las que estamos presentes:
| Cookie | Tipo | Proveedor | Finalidad | Duración |
| _ga_* | No necesaria
Analítica |
Google Analytics | Google Analytics establece esta cookie para almacenar y contar las vistas de página | 1 año 1 mes 4 días |
| _ga | No necesaria
Analítica |
Google Analytics | Instalada por Google Analytics, calcula los datos de visitantes, sesiones y campañas, y también realiza un seguimiento del uso del sitio para el informe analítico. Almacena información de forma anónima y asigna un número generado aleatoriamente para reconocer a los visitantes únicos | 1 año 1 mes 4 días |
| rc::a | Necesaria | google.com | Cookie técnica de seguridad. Esta cookie es establecida por el servicio recaptcha de Google para identificar bots y proteger el sitio web contra ataques maliciosos de spam | Persistente |
| rc::c | Necesaria | google.com | Cookie técnica de seguridad. Esta cookie es establecida por el servicio recaptcha de Google para identificar bots y proteger el sitio web contra ataques maliciosos de spam | Sesión |
| wpEmojiSettingsSupports | Necesaria | seaic.org | Cookie técnica para funcionalidad básica. WordPress establece esta cookie cuando un usuario interactúa con emojis en un sitio de WordPress. Ayuda a determinar si el navegador del usuario puede mostrar emojis correctamente | Sesión |
Google Analytics: Cookies de terceros cuya finalidad es cuantificar el nº de usuarios y así realizar la medición y análisis estadístico del uso que hacen los usuarios de los servicios prestados. Gestionadas por Google, tiene más información en los enlaces sobre el uso de las cookies de Google Analytics y su política de privacidad
Cookies de acceso a Redes Sociales: Twitter, Facebook Youtube Linkedin En cada una de ellas tienes el enlace para poder acceder a más información sobre su política de privacidad y uso de cookies.
Si el usuario enlaza con las redes sociales que compartimos en nuestros portales, le serán instaladas cookies persistentes y de terceros por dicha red social, invitándole a visitar dichas páginas webs para informarse de su política de privacidad, condiciones de uso general o del uso que dan a sus cookies.
Si tiene alguna duda le rogamos nos remita un correo a: rgpd@seaic.org y le responderemos lo antes posible.
¿Se pueden controlar o eliminar las cookies? Sí, y no solo eliminar, también bloquear, de forma general o particular para un dominio específico, si bien igual no podrá acceder a todos los contenidos o que no sea una experiencia de navegación personalizada.
Para eliminar las cookies de un sitio web debe ir a la configuración de su navegador y allí podrá buscar las asociadas al dominio en cuestión y proceder a su eliminación o mediante los siguientes enlaces:
- Eliminación de cookies en Internet Explorer
- Eliminación de cookies en Google Chrome
- Eliminación de cookies en Chrome para Android
- Eliminación de cookies en Mozilla Firefox
- Eliminación de cookies en Safari
- Eliminación de cookies en Safari para IOS(iPhone y iPad)
Más información sobre las cookies: puede consultar más información sobre cookies en el documento publicado por la Agencia Española de Protección de Datos en su “Guía sobre el uso de las cookies” y obtener más información sobre las cookies en Internet, http://www.aboutcookies.org/
Si desea tener un mayor control sobre la instalación de cookies, puede instalar programas o complementos a su navegador, conocidos como herramientas de “Do Not Track”, que le permitirán escoger aquellas cookies que desea permitir.
Política de Privacidad
Política de privacidad
La SOCIEDAD ESPAÑOLA DE ALERGOLOGIA E INMUNOLOGIA CLINICA (SEAIC), como responsable del servicio de los sitios web bajo el dominio seaic.org, y sus subdominios, en adelante el SITIO WEB, quiere ofrecerle las mayores garantías legales en relación con su privacidad y explicarle con la mayor claridad y transparencia posible, todo lo relativo al tratamiento de la información personal que nos proporcione a través de los diferentes sistemas de captura utilizados en nuestros sitios web. Esta política de privacidad ha sido actualizada por última vez el 19/12/2023.
Hemos actualizado esta política con el objetivo de explicarle el tipo de datos personales que recogemos, por qué los recogemos y cómo puede actualizarlos, gestionarlos, exportarlos y eliminarlos. La SEAIC ha adecuado sus sitios web a las exigencias de la Ley Orgánica 3/2018, de 5 de diciembre, de Protección de Datos de Carácter Personal y Garantía de los Derechos Digitales (nueva LOPD), y cumplen también con el Reglamento (UE) 2016/679 del Parlamento Europeo y del Consejo de 27 de abril de 2016 relativo a la protección de las personas físicas (RGPD), así como con la Ley 34/2002, de 11 de julio, de Servicios de la Sociedad de la Información y Comercio Electrónico (LSSICE).
Esta Política tiene la finalidad de ofrecerle toda la información necesaria sobre qué tipo de información personal recopilamos y utilizamos, cómo puede controlar su uso, y describe nuestras prácticas relacionadas con la información recopilada de los diferentes sitios web de la SEAIC que enlazan o hacen referencia a esta Política (como, por ejemplo, páginas de redes sociales y mensajes de correo electrónico con formato HTML).
1. Responsables del tratamiento de sus datos personales
- SOCIEDAD ESPAÑOLA DE ALERGOLOGIA E INMUNOLOGIA CLINICA (SEAIC)
- NIF/CIF: G-58318395
- Dirección: Calle Agustín de Foxá, 25, Chamartín, 28036, Madrid.
- Correo electrónico de contacto: seaic@seaic.org Teléfono: 915 348 826
2. Recogida de datos, finalidades, base de legitimación y plazos de conservación
- Socios. Sus datos serán tratados al haberse dado de alta como socio o mientras no nos comunique su baja, conforme a los fines de los estatutos de la asociación y en base a la prestación de servicios y la ejecución contractual.
Los datos solicitados al socio serán tratados también con la finalidad de tramitar su renovación, de suscribirle a los servicios adicionales ofrecidos, de generar los recibos y el pago (mediante domiciliación en su cuenta bancaria o Paypal) y en general para la gestión de las actividades y eventos de la SEAIC y de sus órganos de representación, la gestión de las relaciones de la SEAIC con terceras personas, jurídicas y físicas, públicas y privadas y la organización de las actividades que la SEAIC desarrolle en cumplimiento de sus fines.
Usted podrá crearse un perfil personal en nuestra área de socios donde podrá acceder mediante usuario y contraseña a sus datos y actualizarlos en cualquier momento.
Los socios registrados se comprometen a mantener actualizados sus datos, sobre todo antes de la renovación anual a inicios de cada año fiscal para actualizar la cuota, en caso de que corresponda hacerlo, y su pago. El socio solo aparecerá en el directorio visible para otros socios y en nuestro directorio “encuentra a tu alergólogo”, si así lo decide.
La SEAIC podrá enviarle información de sus servicios en base al interés legítimo para el cumplimiento de sus fines estatutarios y mantener al socio al tanto de las novedades, actividades, o eventos de la SEAIC o de terceros que pueden ser de interés para el sector. En todo caso, el socio podrá cancelar el envío de nuestras comunicaciones en cualquier momento.
La SEAIC mantendrá sus datos activos mientras sea socio y una vez solicitada su baja los mantendremos bloqueados hasta cinco años más, para atender posibles gestiones tributarias o para cubrir posibles responsabilidades, siempre y cuando no sean aplicables otros plazos. Algunos datos identificativos, profesionales y académicos mínimos, junto con las fechas de alta y baja en la SEAIC serán mantenidos por razones históricas y estadísticas durante toda la vida útil de la propia SEAIC y al objeto de poder emitir certificados que acrediten los años de pertenencia a la SEAIC.
Comités científicos. Usted como socio podrá formar parte de los mismos y participar en los proyectos o publicaciones realizadas, mientras lo desee.
- Participación en convocatoria de ayudas o premios organizados por la SEAIC. La SEAIC, como difusora de la alergología en España, convoca diversas convocatorias de ayudas o premios que cuentan con la participación de socios u otras personas físicas interesadas en participar (pacientes, miembros de asociaciones, etc.). Los concursantes deben facilitar sus datos identificativos, de contacto, así como la información Los concursantes deben facilitar sus datos identificativos, de contacto, así como la información establecida en las bases de cada convocatoria, que deberán de consultar. La base del tratamiento de sus datos se sustenta en la prestación del servicio para llevar a cabo la evaluación y resolución del concurso por parte de un Jurado
La SEAIC podrá publicar en medios de comunicación la relación de ganadores, así como imágenes y reseñas de los actos celebrados en base al interés legítimo. Al referirse a menores de edad, en la mayoría de los casos, se optará por la publicación únicamente de sus iniciales acompañadas por el centro al que pertenecen.
Los datos de los concursantes serán conservados durante 2 años, salvo los datos identificativos de los ganadores que serán mantenidos por razones históricas y estadísticas durante toda la vida útil de la propia SEAIC.
- Inscripciones a congresos. Como socio, usted puede inscribirse a nuestro congreso anual organizado por la SEAIC, debiendo hacerlo mediante la página web que nuestro colaborador Viajes El Corte Inglés habilite con la finalidad de tramitar su inscripción al congreso, gestionar el cobro y enviarle la información y servicios sobre el mismo. Viajes El Corte Inglés, como Encargado del Tratamiento, únicamente tratará los datos mínimos y necesarios para prestarnos dichos servicios.
- Cursos. Los socios podrán contratar alguno de los cursos ofertados por la SEAIC debiendo cumplimentar el formulario habilitado a tal efecto facilitando sus datos ident0ificativos y de contacto, e información de pago y facturación.
La base de legitimación es la relación contractual o prestación del servicio y los datos facilitados serán conservados mientras se mantenga dicha relación, así como bloqueados hasta cinco años más, por gestiones tributarias y para cubrir posibles responsabilidades.
De no existir plazas disponibles para el curso seleccionado, el usuario puede facilitar su correo electrónico, prestando su consentimiento para ser incluido en una lista de espera y ser contactado, por la SEAIC, a efectos de ser informado de nuevas convocatorias. Su correo electrónico será conservado hasta la siguiente convocatoria del curso o, en su defecto, durante un plazo máximo de 1 año.
- Premios anuales otorgados por la SEAIC. Los candidatos deben facilitar sus datos identificativos, de contacto, y los vinculados a sus méritos para evaluar su candidatura. La base del tratamiento de sus datos se sustenta en la prestación del servicio para llevar a cabo la evaluación y concesión de los premios por parte de un Jurado según la normativa que figura en la convocatoria de los premios, así como para gestionar el envío de comunicaciones, noticias o de próximos eventos, siempre y cuando usted nos de su consentimiento. Los méritos de los candidatos serán compartidos exclusivamente con los evaluadores que formen parte del Jurado.
La SEAIC podrá publicar en medios de comunicación la relación y fotografías de los premiados, así como imágenes y reseñas de los actos celebrados en base al interés legítimo. La imagen, el nombre y apellidos de los premiados serán compartidos con los patrocinadores de los premios.
Los datos de los candidatos serán conservados durante 2 años y transcurridos los plazos de conservación o bloqueo de datos, los datos personales serán eliminados conforme a nuestras políticas internas, salvo los datos identificativos de los premiados que serán mantenidos por razones históricas y estadísticas durante toda la vida útil de la propia SEAIC.
Para la participación en las ceremonias de entrega de los premios se recogerán datos identificativos de los asistentes, que serán eliminados en el plazo de dos meses desde la fecha del evento.
- Inscripciones a eventos. Usted puede inscribirse en los eventos que periódicamente organiza la SEAIC como socio o usuario no asociado, debiendo facilitar sus datos identificativos y de contacto, así como, en caso de que no se trate de un evento gratuito, información de pago y facturación.
La base jurídica del tratamiento de sus datos se sustenta en la prestación del servicio y la ejecución contractual necesaria para formalizar la inscripción y participación en los eventos. Si el evento es gratuito sus datos personales serán tratados con el fin de gestionar su inscripción y asistencia, y también con la finalidad de gestionar el envío de comunicaciones, noticias o de próximos eventos, siempre y cuando usted nos dé su consentimiento.
Si el evento es gratuito, sus datos serán conservados durante un año, salvo que sean aplicables otros plazos. Si es de pago, transcurrido un año serán bloqueados hasta cinco años más, para atender posibles gestiones tributarias o para cubrir posibles responsabilidades, siempre y cuando no sean aplicables otros plazos.
- Conferenciantes y profesores. Los conferenciantes y profesores invitados a impartir una charla/curso y quienes así lo soliciten, deben facilitar sus datos identificativos y de contacto. La base del tratamiento de sus datos se sustenta en la prestación del servicio de organización de eventos y cursos. Deberán facilitar su consentimiento con la firma del documento titulado habilitado para tal fin.
La SEAIC podrá publicar en medios de comunicación la relación conferenciantes y profesores, la institución a la que pertenecen, así como el título de sus charlas o cursos en base al interés por la difusión de la actividad. En aquellos casos en los que así se determine, se les podrá solicitar una foto siempre y cuando Usted nos de su consentimiento.
Los datos de los conferenciantes/profesores serán conservados durante dos años y luego bloqueados hasta cinco años más, para atender posibles gestiones tributarias o para cubrir posibles responsabilidades, siempre y cuando no sean aplicables otros plazos. Los datos de los ganadores que serán mantenidos por razones históricas y estadísticas durante toda la vida útil de la propia SEAIC
Algunos datos identificativos serán mantenidos por razones históricas y estadísticas durante toda la vida útil de la propia SEAIC y al objeto de poder emitir certificados que acrediten la actividad realizada.
- Boletín o suscripción a boletines. Los usuarios no asociados podrán suscribirse a nuestros boletines informativos a través del correo electrónico, solicitándole los siguientes datos personales: nombre, apellidos y correo electrónico, que trataremos en base al consentimiento solicitado. Sus datos de contacto serán conservados para esta finalidad mientras no cancele su suscripción.
- Formulario de contacto. Nos pondremos en contacto con usted, a través de correo electrónico para atender su consulta o responder a las preguntas que nos haga a través de nuestra web, teléfono o direcciones de correo electrónico. Le solicitamos los siguientes datos personales: nombre, apellidos y correo electrónico, que trataremos en base al consentimiento solicitado. En todos los casos se usará la dirección de correo electrónico para responderle. Sus datos de contacto serán conservados para esta finalidad durante un año, salvo que sean aplicables otros plazos.
Tratamiento de imágenes
Como normal general, la SEAIC puede grabar su imagen en los distintos eventos o actividades que realiza, ya que de manera general dichos actos son grabados con la finalidad usarlos como medio de promoción y difusión de la SEAIC o por su carácter de interés general, informativo y/o divulgativo, pudiéndolos publicar en nuestra página web, redes sociales, prensa o televisión en base al interés legítimo.
No obstante, en las bases y/o convocatoria del evento o actividad, se informará sobre el tratamiento de sus datos, incluida la imagen y se solicitará el oportuno consentimiento en el momento de la inscripción, sobre todo en aquellas actividades que no tengan ese carácter de interés general, informativo y/o divulgativo.
En cualquier caso, Usted también será informado al inicio del evento sobre esta circunstancia y si Usted no nos da su consentimiento, deberá ubicarse en la zona de la sala que le indicaremos. Del mismo modo, si en dicho evento hubiese otros actos, anteriores o posteriores al evento central o principal, es decir, de recepción, Cóctel, etc. Aunque el fotógrafo le preguntará, le rogamos recuerde decirle al fotógrafo que no desea salir en dichas fotos.
En todos los casos el tratamiento de las imágenes se hará de conformidad con lo establecido en la L.O. 1/1982, de 5 de mayo, de Protección Civil del Derecho al Honor, a la Intimidad Personal y Familiar y a la Propia Imagen, cuya cesión tendrá carácter gratuito y en ningún caso comportará la obligación de que usemos dichas imágenes.
Información adicional sobre el tratamiento de datos personales:
- Revocabilidad: En los casos en los que la SEAIC solicite su consentimiento, éste es revocable en cualquier momento comunicándolo a la SEAIC en los términos establecidos en esta política para el ejercicio de los derechos. La revocación que no tendrá carácter retroactivo.
- Transcurridos los plazos de conservación o bloqueo de datos, todos los datos personales tratados por la SEAIC serán eliminados conforme a nuestras políticas internas, asegurándonos que no se puede reconstruir ni leer excepto algunos datos de los socios. Dichos datos serán los identificativos, profesionales y académicos mínimos, que junto con las fechas de alta y baja en la SEAIC serán mantenidos por razones históricas y estadísticas durante toda la vida útil de la propia Asociación y al objeto de poder emitir certificados que acrediten los años de pertenencia a la Asociación.
- No aceptamos el envío de CV en nuestro formulario de contacto o de manera espontánea a nuestros correos electrónicos, por lo que cualquier archivo remitido en este sentido será inmediatamente eliminado.
Existen otras finalidades para las cuales tratamos sus datos personales:
- Para garantizar el cumplimiento de las condiciones de uso y la ley aplicable. Esto puede incluir el desarrollo de herramientas y algoritmos que ayudan a esta web a garantizar la confidencialidad de los datos personales que recoge.
- Para apoyar y mejorar los servicios que ofrece el SITIO WEB.
- Cookies. Nuestro SITIO WEB dispone de tecnología para la implantación de archivos en el equipo del usuario. Dichos archivos, denominados “cookies”, tienen diferentes finalidades y son instaladas previo consentimiento, pudiendo usted bloquear o deshabilitarlas a través de las opciones de configuración de su navegador. Dispone de toda la información detallada en nuestra política de cookies.
- Para gestionar las redes sociales en las que la SEAIC tenga presencia. El tratamiento de los datos que se lleve a cabo de las personas que se hagan seguidoras en las redes sociales de las páginas oficiales de la SEAIC, se regirá por este apartado. Así como por aquellas condiciones de uso, políticas de privacidad y normativas de acceso que pertenezcan a la red social que proceda en cada caso y aceptadas previamente por el usuario. La SEAIC tratará sus datos con las finalidades de administrar correctamente su presencia en la red social, informándole de nuestras actividades, productos o servicios, así como para cualquier otra finalidad que las normativas de las redes sociales permitan.
En ningún caso utilizaremos los perfiles de seguidores en redes sociales para enviar publicidad de manera individual. La SEAIC no vende, alquila ni cede datos de carácter personal que puedan identificar al usuario, ni lo hará en el futuro, a terceros sin el consentimiento previo.
Exactitud y veracidad de los datos: Como socio o usuario, es usted el único responsable de la veracidad y corrección de los datos que nos remita, exonerando a la SEAIC de cualquier responsabilidad al respecto. Usted garantiza y responde, en cualquier caso, de la exactitud, vigencia y autenticidad de los datos personales facilitados, comprometiéndose a mantenerlos debidamente actualizados.
Aceptación y consentimiento: El usuario declara haber sido informado de las condiciones sobre protección de datos de carácter personal, aceptando y consintiendo el tratamiento de estos por parte de la SEAIC en la forma y para las finalidades indicadas en esta política de privacidad.
Comunicaciones o correos comerciales: De acuerdo con la LSSICE, la SEAIC no realiza prácticas de SPAM, por lo que no envía comunicaciones o correos comerciales por vía electrónica que no hayan sido previamente solicitados o autorizados por el usuario. En consecuencia, en cada uno de los formularios habidos en los distintos sitios web de la SEAIC, el usuario tiene la posibilidad de dar su consentimiento expreso para inscribirse al boletín, cuya comunicación estará debidamente identificada, con independencia de la información puntualmente solicitada.
3. Socios: proceso y condiciones de registro o suscripción y pago de cuotas
La SEAIC no admite la suscripción por parte de menores de edad, de manera que, si la fecha de nacimiento señala que es menor de 18 años, no se procederá a la tramitación de su alta ni al cobro de la cuota.
El proceso de alta en la SEAIC se inicia cuando la persona interesada en ser socio de la SEAIC envía el formulario de solicitud de inscripción. Una vez recibido, desde nuestra Secretaría Técnica revisamos la información suministrada y comprobamos la cuota correspondiente. Posteriormente, notificamos a través del correo electrónico al nuevo socio que su inscripción ha sido validada, le informamos sobre el pago y le orientamos sobre cómo crear su perfil personal en el área de socios y/o acceder al mismo.
La suscripción/renovación como socio de la SEAIC se realiza mediante el pago de una cuota anual que podrá efectuarse por domiciliación bancaria o mediante el pago con Paypal.
El proceso de pago se llevará a cabo mediante una de estas dos modalidades:
- Domiciliación a su cuenta bancaria. Usted recibirá un correo electrónico para confirmarle el próximo cobro de la cuota y su cuantía, al menos con una semana de antelación al cobro. El cargo se realizará de forma automática en su cuenta en tanto no notifique su intención de ser baja de la SEAIC. La domiciliación bancaria es la forma de pago más recomendable, ya que facilita el trabajo administrativo de la Secretaría Técnica.
- PAYPAL. Usted recibirá un correo electrónico con el recibo correspondiente y un enlace a la pasarela de pago, externa a la SEAIC. Debe realizar el pago por sí mismo y aceptar las políticas de la pasarela de pago externas a la SEAIC que en ningún caso almacenará o tratará los datos de su tarjeta.
Los socios registrados se comprometen a mantener actualizados sus datos, sobre todo antes de la renovación anual a inicios de cada año fiscal para actualizar la cuota, en caso de que corresponda hacerlo, y su pago.
Las cuotas, así como los recibos correspondientes, estarán disponibles en el perfil del socio de la SEAIC. Quienes necesiten factura en lugar del recibo podrán solicitarla a seaic@seaic.org, una vez hayan realizado el pago.
Políticas de retorno, devolución y cancelación
Un socio se podrá dar baja de la SEAIC en cualquier momento. Para ello debe contactar con la Sociedad a través del correo seaic@seaic.org. Una vez realizado el pago de la cuota del año en curso, a los socios que se den baja de la SEAIC o de un grupo no se les devolverá el importe correspondiente.
4. Navegación
Al navegar por la web se pueden recoger datos no identificables, que pueden incluir, direcciones IP, ubicación geográfica (aproximadamente), un registro de cómo se utilizan nuestros servicios y sitios, y otros datos que no pueden ser utilizados para identificar al usuario. Entre los datos no identificativos están también los relacionados a sus hábitos de navegación a través de servicios de terceros detallados en el apartado Cookies.
5. Secreto y seguridad de los datos
La SEAIC se compromete en el uso y tratamiento de los datos incluidos personales de los usuarios, respetando su confidencialidad y a utilizarlos de acuerdo con la finalidad del mismo, así como a dar cumplimiento a su obligación de guardarlos y adaptar todas las medidas para evitar la alteración, pérdida, tratamiento o acceso no autorizado (como los protocolos Https que usamos), de conformidad con lo establecido en la normativa vigente de protección de datos.
La SEAIC no puede garantizar que la red de Internet sea totalmente inexpugnable y por tanto tampoco que los datos no puedan ser violados mediante accesos fraudulentos a ellos por parte de terceros.
Confidencialidad del procesamiento: La SEAIC se asegurará de que cualquier persona que esté autorizada por nuestra Sociedad para procesar sus datos como socio o usuario (incluido su personal, colaboradores y prestadores) estarán bajo la obligación apropiada de confidencialidad, ya sea un deber contractual o legal.
Respuesta ante un incidente de seguridad: Al darse cuenta de un Incidente de Seguridad, la SEAIC deberá notificárselo al socio o usuario sin demoras indebidas y deberá proporcionar la información oportuna relacionada con el Incidente de Seguridad tal como se conozca o cuando el socio o usuario lo solicite razonablemente.
6. ¿A qué destinatarios se comunicarán sus datos?
Los datos personales sólo serán comunicados a terceros para cumplir con las obligaciones legales, por ejemplo, la tributaria, o en la medida necesaria para la prestación de los servicios y actividades al socio de la SEAIC.
El sitio web de la SEAIC puede dar acceso a otras páginas web, incluidos los perfiles oficiales de la SEAIC en Redes Sociales, informándole que al pulsar en dichos enlaces será redireccionado a una página respecto de la cual la SEAIC no es responsable. Usted debe ser consciente de que estas webs externas a la SEAIC pueden recoger, utilizar o transferir sus datos personales bajo condiciones y términos diferentes, recomendándole que cuando acceda a una de estas páginas web, se informe de su política de privacidad, condiciones de uso general o del uso que pueden dar a sus cookies pues no podemos controlar la forma en que esas páginas webs usan la información personal que usted divulga.
La SEAIC le comunica que realizará encargos de tratamientos a terceros conforme al RGPD, exigiendo por parte del encargado el cumplimiento de todas las garantías de protección de datos. Todas las utilidades ofrecidas por terceros son estrictamente necesarias para el desarrollo de nuestros servicios y han sido seleccionados atendiendo al cumplimiento de los derechos que preservamos en esta web.
Dichas empresas o entidades tendrán acceso a la información personal necesaria para realizar sus funciones como encargados de tratamiento, pero no podrán utilizarla para otros fines. Además, deberán tratar la información personal de conformidad con la presente Política de Privacidad y la legislación aplicable en materia de protección de datos, no realizando trasferencia internacional de los datos que la SEAIC trata.
Hosting: Informarle que el alojamiento de los sitios web de la SEAIC están contratados con Dinahosting SL cuyos servidores están ubicados en España.
Servicios de análisis: Google Analytics (cookies). Un servicio analítico de web prestado por Google, Inc., una compañía de Delaware cuya oficina principal está en 1600 Amphitheatre Parkway, Mountain View (California), CA 94043, Estados Unidos (“Google”). Google Analytics utiliza “cookies”, que son archivos de texto ubicados en su ordenador, para ayudar a la SEAIC a analizar el uso que hacen los usuarios de sus sitios web. La información que genera la cookie acerca de su uso en www.seaic.org (incluyendo su dirección IP) será directamente transmitida y archivada por Google en los servidores de Estados Unidos. Usted podrá aceptar o rechazar la instalación de las cookies de Google Analytics.
7. ¿Cuáles son sus derechos cuando nos facilita sus datos?
Puede ejercer de manera gratuita los derechos que le confiere el RGPD. Cualquier persona tiene derecho a revocar el consentimiento, solicitar el acceso a los datos personales que le conciernen, a solicitar su rectificación o supresión, a solicitar la limitación de su tratamiento, a oponerse a su tratamiento (si hay interés público o interés legítimo) y/o el derecho de portabilidad. En todos los casos podrá ejercer sus derechos por escrito a calle de Agustín de Foxá, 25, Chamartín, 28036, Madrid o por correo electrónico dirigido a rgpd@seaic.org indicando la referencia “Protección de Datos”. En la solicitud debe constar: Nombre, apellidos y fotocopia de su DNI, en caso de serle requerido para acreditar debidamente su identidad, petición en la que se concreta tu solicitud y domicilio/email a efectos de notificaciones. Cualquier persona puede presentar una reclamación ante la Agencia Española de Protección de Datos a través de la web www.agpd.es en caso de considerar que sus derechos no han sido satisfechos.
8.Resolución de conflictos
Si tiene alguna queja relacionada con nuestro cumplimiento de esta política de privacidad, debe contactar con nosotros en primer lugar. Investigaremos e intentaremos resolver las quejas y conflictos en relación con el uso y divulgación de la información personal de acuerdo con esta política.
TRATAMIENTO BIOLÓGICO EN LAS ENFERMEDADES ALÉRGICAS/ASMA GRAVE
Los medicamentos biológicos son producidos por organismos vivos o a partir de ellos (microorganismos humanos, animales o células de biotecnología) y se caracterizan por su alta especificidad y actividad terapéutica porque van dirigidos a la proteína o al receptor concreto que interviene en el proceso de la enfermedad.
Se consideran productos biológicos a las vacunas, alérgenos, antígenos, hormonas, inmunoglobulinas, citocinas, derivados de la sangre o plasma y anticuerpos monoclonales, entre otros.
Su auge se debe al gran avance de la biología molecular a través de técnicas de DNA recombinante, al conocimiento del genoma humano y de las vías de regulación de la respuesta inmune, que ha permitido identificar un variado número de dianas o puntos clave para este tipo de terapia.
El descubrimiento y producción de anticuerpos monoclonales (Ac Mo) por el Dr. Milstein en 1975 ha marcado la historia de la Medicina y Biotecnología. Inicialmente la indicación terapéutica se centró en áreas como reumatología y oncología, extendiéndose a diversas especialidades médicas como aparato digestivo, neurología, y también a la alergología.
La incorporación de anticuerpos monoclonales (Ac Mo) a la terapia alergológica ha significado un avance significativo en la medicina personalizada y de precisión, mejorando el manejo de las enfermedades alérgicas. Actúan bloqueando reguladores del sistema inmunitario claves en estas enfermedades.
Hasta el momento, en Alergología, los fármacos biológicos están indicados en:
- Asma Grave (Escalón 5-6 de la GEMA)
- Dermatitis Atópica
- Urticaria Crónica
- Esofagitis Eosinofílica, Síndrome Hipereosinofílico (SHE)
- Granulomatosis eosinofílica con poliangeítis (GEPA)
- Rinosinusitis Crónica con Poliposis Nasal (RSNCcPN)
- Angioedema Hereditario
Están en estudio algunos fármacos biológicos como tratamiento adyuvante en procesos de desensibilización con alimentos o medicamentos o inmunoterapia de alto riesgo, entre otros.
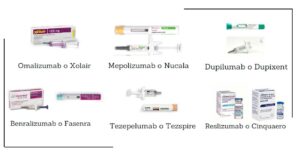 Imagen 1. Ejemplo de fármacos biológicos utilizados en alergología en la actualidad
Imagen 1. Ejemplo de fármacos biológicos utilizados en alergología en la actualidad
En general, el tratamiento biológico reduce los síntomas, disminuye el uso de glucocorticoides orales, así como los ingresos hospitalarios, lo que conlleva menos costes sanitarios. Además, mejora el control de la enfermedad y la calidad de vida del paciente.
La administración del fármaco se realiza en un centro sanitario (hospital o Centro de Salud) por enfermeras o bien se instruye y educa al paciente para que se pueda autoadministrar el fármaco en su domicilio, cuando la vía de administración es la subcutánea, ya que existen jeringas y plumas precargadas y preparadas para la inyección .
EFECTOS ADVERSOS MÁS HABITUALES
ADMINISTRACIÓN DOMICILIARIA
La enfermera, como educadora en autocuidados, es la encargada de evaluar si el perfil del paciente es adecuado para garantizar la seguridad de la administración, conservación, técnica adecuada y el cumplimiento del tratamiento en su domicilio.
Para ello, la enfermera, durante las primeras dosis administradas en el centro sanitario, educa y valora al paciente/cuidador en relación a los siguientes aspectos: Conservación, preparación, localización de la zona y la técnica correcta de inyección, efectos adversos y eliminación del residuo.
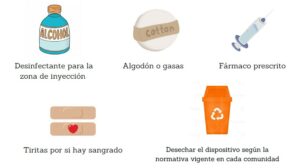
PRECAUCIONES A TENER EN CUENTA ANTES DE LA ADMINISTRACIÓN
- Mantener el medicamento fuera de la vista y del alcance de los niños.
- No utilizar el medicamento después de la fecha de caducidad que aparece en el etiquetado.
- Conservar en nevera (entre 2-8º). No congelar ni calentar.
- Conservar en el embalaje original (esto lo protege de la luz).
- El envase que contiene el dispositivo precargado puede conservarse a temperatura ambiente (25º), antes de usarlo, de horas a días en función del biológico que tenga prescrito el paciente.
- No utilizar ningún envase que esté dañado o muestre indicios de deterioro.
- Visualizar el aspecto del fármaco antes de utilizarlo (que muestre un aspecto claro sin turbideces).
- No agitar el dispositivo precargado.
MATERIAL NECESARIO PARA LA AUTOADMINISTRACIÓN
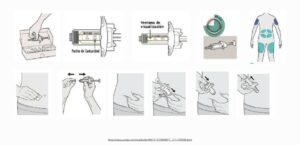
PASO A PASO AUTOADMINISTRACIÓN
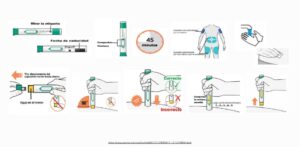
PLUMA PRECARGADA
JERINGA PRECARGADA
BIBLIOGRAFÍA
- Cuñetti L. Generalidades de los Medicamentos Biológicos [Internet]. Boletín farmacológico. 2014 [citado agosto 2024]. Disponible en: http://www.boletinfarmacologia.hc.edu.uy/index.php?option=com_content&task=view&id=104&Itemid=66
- Gema 5.4. Guía española para el manejo del asma. [Internet]. Madrid: Ed. Luzán 5; 2024. [citado agosto 2024]. Disponible en: http://.www.gemasma.com
- Iniciativa estratégica para el abordaje integral del asma: resumen ejecutivo. Disponible en : https://.seaic.org/profesionales/noticias-para-profesionales/libro-asma360.html (consultado julio 2024)
- Sabaté Brescó M, Salas Cassinello M, Sánchez Hernández MC, Sánchez Machín I, Sánchez Matas I, Sastre Domínguez J et al. El libro de las enfermedades alérgicas. [Internet]. Madrid: Fundación BBVA; 2021[citado agosto 2024]. Disponible en: https://www.fbbva.es/wp-content/uploads/2021/10/Libro-enfermedades-alergicas_FBBVA.pdf
- Delgado Romero J , Blanco-Aparicio M , Cisneros Serrano C , Díaz-Pérez D, Ferrando Piqueres R, López-Carrasco V, Merino-Bohórquez V , Soto-Retes L , Domínguez-Ortega J. Apoyo a la administración domiciliaria de terapia biológica en pacientes con asma grave: BioCart© [Internet].J Investig Allergol Clin Immunol 2022; Volumen 32(6): 482-484. Doi: 10.18176/jiaci.0786
- Ficha técnica autorizada de Xolair ® (omalizumab) (Consultado en septiembre 2024) Disponible en: https://cima.aemps.es/cima/dochtml/ft/05319008/FT_05319008.html
- Ficha técnica autorizada de Nucala® (mepolizumab) (Consultado en septiembre 2024)Disponible en: https://cima.aemps.es/cima/dochtml/ft/1151043001/FT_1151043001.html
- Ficha técnica autorizada de Fasenra ® (benralizumab) (Consultado en septiembre 2024)Disponible en : https://cima.aemps.es/cima/dochtml/p/1171252001/P_1171252001.html
- Ficha técnica autorizada de Dupixent® (dupilumab) (Consultado en septiembre 2024) Disponible en : https://cima.aemps.es/cima/dochtml/ft/1171229006/FT_117229006.html
- Ficha técnica autorizada de Tezspire® (tezepelumab) (Consultado en septiembre 2024) Disponible en: https://cima.aemps.es/cima/dochtml/ft/1221677001/FT_1221677001.html
Comunidad Valenciana
Comunidad valenciana
Centros con actividad asistencial pública en Alergología
Alicante
Hospital de Alcoy "Virgen del los Lirios"
- http://www.a14.san.gva.es
- Polígono Caramanxell, s/n. 03804 Alcoy
- 965537400
Hospital de Orihuela "Vega Baja"
- http://www.dep21.san.gva.es
- Ctra. Orihuela-Almoradí, s/n (Ptda.S.Bart) 03314 Orihuela
- 965877500
Hospital de Villajoyosa "Marina Baixa"
- Sitio web no disponible
- Avda. Alcalde En Jaume Botella Mayor, 7. 03570 Villajoyosa
- 966859800
Hospital de Denia "Marina Salud"
- http://www.marinasalud.es
- Partida Beniadlá, s/n. 03700 Denia
- 966429000
Hospital del Vinalopó
- http://www.vinaloposalud.com
- Tónico Sansano Mora, 14. 03293 Elche
- 966 67 98 00
Hospital General de Elda "Virgen de la Salud"
- http://www.elda.san.gva.es
- Ctra. Elda-Sax. Ptda La Torreta. 03600 Elda
- 966989000
Hospital General Universitario de Alicante
- http://www.dep19.san.gva.es
- C/ Pintor Baeza, 12. 03010 Alicante
- 965933000
Hospital General Universitario de Elche
- http://www.dep20.san.gva.es
- C/ Camino de la Almazara, 11. 03203 Elche
- 966616900
Hospital de Torrevieja
- http://www.torrevieja-salud.com
- Ctra. CV-95 Torrevieja-S.Miguel de Salinas.Ptda Ceñuela. 03186 Torrevieja
- 965721313
Castellón
Hospital de La Plana
- http://www.laplana.san.gva.es
- Ctra. Villarreal-Borriana, km 0,5. 12540 Villarreal
- 964357600
Hospital Universitario General de Castellón
- http://www.castello.san.gva.es/
- Avda. Benicasim, s/n. 12004 Castellón de la Plana
- 964726500
Valencia
Consorcio Hospital General Universitario de Valencia
- http://chguv.san.gva.es
- Avda. tres Cruces, s/n. 46014 Valencia
- 961972000
Hospital Arnau de Vilanova – Valencia
- Sitio web no disponible
- C/ San Clemente, 12. 46015 Valencia
- 963868501
Hospital Clínico Universitario de Valencia
- Sitio web no disponible
- Avda. Blasco Ibáñez, 17. 46010 Valencia
- 963862600
Hospital La Ribera de Alzira
- http://www.hospital-ribera.com
- Ctra. Corbera, km. 1. 46600 Alcira
- 962458100
Hospital Lluís Alcanyís
- http://www.xativaontinyent.san.gva.es
- Crta. Xátiva-Silla, km 2. 46800 Xátiva
- 962289500
Hospital Universitario Doctor Peset
- Sitio web no disponible
- Avda. Gaspar Aguilar, 90. 46117 Valencia
- 961622300
Hospital Universitari i Politècnic La Fe
- http://www.hospital-lafe.com/
- http://www.alergialafe.org/
- Avda. Fernando Abril Martorell, 106. 46026 Valencia
- 961244083
Los Bomberos crean un protocolo para neutralizar los riesgos de las abejas
Fuente: V. López Del Tell (Elche) para http://www.diarioinformacion.com
El suboficial del Parque de Elche diseña un plan que se aplica en toda la provincia basado en la formación para atajar colmenas y enjambres.
Los Bomberos han normalizado sus actuaciones para hacer frente a los riesgos de las abejas mediante un protocolo que están aplicando los parques de toda la provincia. El suboficial jefe del área operativa del Baix Vinalopó, José Soler Bonet, ha sido el encargado de diseñar un plan que ha fijado las pautas de actuación y el material necesario para neutralizar las colmenas silvestres y los enjambres cuando pueden ser peligrosos para las personas.
Los Bomberos han tenido que adaptarse a los nuevos tiempos para poder ofrecer el servicio de recogida de enjambres y colmenas de una forma racional y compatible con la sostenibilidad. «La crisis de la miel provocó que, en una zona como la nuestra donde prima el turismo, las urbanizaciones e infraestructuras, descendiera mucho el número de apicultores», explica el suboficial. En los años 80 y 90 los Bomberos disponían de una lista de apicultores muy extensa a la que recurrían cuando un ciudadano daba aviso de una situación peligrosa a causa de las abejas. «El número de profesionales se redujo tanto, y los pocos que había no podían acudir principalmente por sus quehaceres profesionales, que tuvimos que ponernos al día, porque los problemas de este tipo siempre acababan en nuestra centralita», asegura José Soler.
Necesidad
La demanda de los ciudadanos encontró respuesta en este bombero aficionado a la apicultura. «Aprendimos de los profesionales y de los libros. Teniendo en cuenta que la abeja es una especie protegida no podíamos llegar y destruir las colmenas sin más, así que nos preparamos hasta normalizar el servicio», expone Soler. Él es el encargado de ofrecer una acción formativa entre los bomberos de toda la provincia para que estén preparados para actuar en caso de urgencia. «Lo primero que hacemos siempre es avisar a los apicultores que nos han facilitado sus contactos, porque no se trata de quitarle a nadie el trabajo. De hecho, seguimos animando a que los interesados nos llamen para tener sus teléfonos en la base de datos», afirma el suboficial, quien recuerda al ciudadano que «este tipo de servicios generan unas tasas, por lo que al final es mejor que los realice un profesional».
Otro punto que el responsable del servicio quiere dejar claro a los ciudadanos es que «la neutralización sólo la realizamos cuando hay un enjambre o una colmena de abejas, por ser una especie protegida. Para tratar los problemas generados por avispas u otros insectos no protegidos, existen empresas de desinsectación que se encargan de ello», apunta el responsable del Parque de Bomberos de Elche-Baix Vinalopó. En la comarca se atienden cada año más de 80 casos de abejas, «destacando lógicamente los meses de primavera». Hay que tener en cuenta que las abejas, cuando la colmena se hace muy grande o una reina es expulsada y se lleva consigo a parte de la colonia, se marchan a otro sitio buscando el lugar más idóneo para su asentamiento. «Pueden estar hasta tres días en forma de enjambre, que es cuando vemos como una pelota de abejas que lo que hacen es proteger a su reina y llevarla a un lugar tranquilo y donde haya alimento», explica el responsable de la unidad, quien recalca que «para hacer ese transporte eligen los meses de mejor climatología».
Cuando los Bomberos reciben una llamada de alerta, primero valoran si es un enjambre (multitud de abejas con su maestra, que juntas salen de una colmena para formar otra colonia) o de una colmena silvestre (recipiente construido para habitáculo de las abejas). El enjambre es menos peligroso que la colmena. «En él las abejas no están en su casa y, por tanto, no tienen el sentido de proteger su territorio. Están de paso y, por ello, se pueden encontrar enjambres en lugares tan extraños como un semáforo, árboles de parques, bancos o un espejo de coche», afirma Soler. En un reciente parte de novedades de la Policía Local de Elche se cita textualmente: «Detección de un panal de abejas en la parte posterior de una motocicleta, cuyo conductor se percató de ello cuando se encontraba en marcha, deteniéndose de inmediato, dando aviso a los Bomberos».
Peligrosidad
Este tipo de casos, que parecen más propios del cine que de la realidad, «se dan porque las abejas, cuando están cansadas y cae la noche, se resguardan para con el alba volver a buscar el lugar para su asentamiento definitivo». En estos casos «el peligro es menor también porque esas abejas se han alimentado más de lo normal para soportar dos o tres días de viaje y llevan el buche lleno, lo que les impide hacer el movimiento para picar. Además, guardan sus fuerzas para buscar su sitio. Los enjambres no atacan si tú no los atacas», asegura Soler.
El caso de la colmena silvestre (distinta a la racional que utilizan los apicultores para producir jalea, miel y cera) es más complejo. «Fue famoso el caso de la basílica de Santa María. Allí se formó una colmena inmensa bajo unas tablas de madera», cuenta el bombero, quien apunta que «las abejas buscan lugares tranquilos, donde pase muy poca gente». Otro caso que Soler recuerda se dio en un chalé de Matola. «Las casas de campo que son ocupadas sólo en verano suelen ser sitios frecuentados por las abejas, que forman sus colonias principalmente en chimeneas, grietas, hasta en un «colombaire» encontramos hace semanas una colmena», afirma José Soler.
La forma de actuar de los Bomberos se ha profesionalizado. Además del vestuario de protección adecuado, utilizan enseres propios de la apicultura para introducir en cajas a las abejas, «que después soltamos en lugares apartados, en plena naturaleza». Además, usan ahumadores para adormilar al insecto y feromonas para atraer su atención hacia el recipiente. Cuando la colmena ya se ha trasladado, rocían su antigua colmena con gasoil o vinagre para evitar su regreso. «En poco más de media hora podemos retirar la colmena en casos normales. En la basílica de Santa María necesitamos mucho más tiempo porque allí se recogieron el triple de abejas de lo normal».
Captador de la semana: Jaén

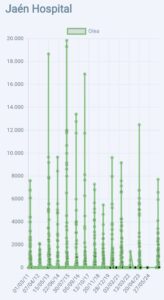
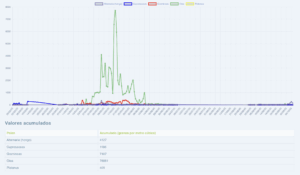
Toca presentar al Dr. Juan Luis Anguita Carazo, responsable del captador de la red SEAIC localizado en el Hospital Universitario de Jaén, donde el Dr. Anguita junto con el resto de compañeros del servicio realizamos los contajes de pólenes desde el 2011.

Jaén, mar de olivos, alcanzó el record histórico de conteo de polen de olivo diario en mayo del 2015 con 19.840 granos por metro cúbico de aire.
El Dr. Anguita ha realizado para esta ocasión dos interesantes videos donde podréis conocer la historia de este captador así como a todos los compañeros que actualmente colaboran con los contajes.
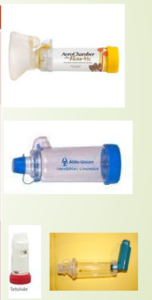
CÁMARAS DE INHALACIÓN
No son dispositivos de inhalación propiamente dichos, pero su utilización está ampliamente recomendada para evitar problemas relacionados con la técnica de los inhaladores de cartucho presurizado. Es un espaciador que separa la boquilla del cartucho presurizado de la boca del paciente. Por este motivo antiguamente se denominaban a estos aparatos “espaciadores” y hoy en día se utilizan ambos nombres de manera indistinta (cámaras de inhalación o cámaras espaciadoras)
Poseen una válvula en su boquilla habitualmente unidireccional que permite la inspiración del aire de la cámara, pero no la espiración dentro de ella.
Su uso enlentece la velocidad de salida del aerosol y evapora el propelente. Las partículas de aerosol pequeñas se mantienen unos segundos en suspensión en espera de ser inhaladas, y las grandes chocan con las paredes de la cámara y quedan retenidas. De esta forma se produce un menor depósito orofaríngeo y se aumenta el depósito pulmonar. El uso de la cámara inhalatoria permite utilizar menor cantidad de fármaco, reduciendo los efectos secundarios, tanto sistémicos como locales y, por eso, se aconseja en caso de disfonía debida al uso de los inhaladores. Además, eliminan la dificultad de coordinar la inspiración con la pulsación del dispositivo.
Se utilizan en el tratamiento de las exacerbaciones de asma (excepto las de riesgo vital), ya que el efecto broncodilatador administrado con cámara de inhalación es equivalente al de un nebulizador y es una alternativa en pacientes con bajo flujo inspiratorio.
Al igual que con los diferentes inhaladores es importante adiestrar al paciente en el uso de la cámara inhalatoria y revisar la técnica periódicamente.
Tipos de cámaras
Existen cámaras de diferentes tamaños desde 140-800 ml. Son universales, permitiendo su conexión a los diferentes modelos de inhaladores de cartucho presurizado, son portátiles y se pueden utilizar con mascarillas faciales. 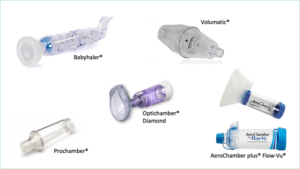
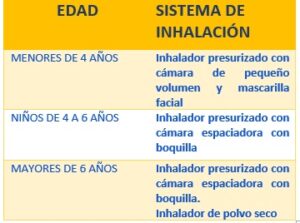
Recomendaciones de uso de dispositivos de inhalación según edad
Elaboración propia (Modificado de GEMA- Inhaladores,2018)
Limpieza y mantenimiento de las cámaras
- Son de uso personal
- Limpiar semanalmente, si se usa a diario, con agua templada y detergente suave o neutro, separando las piezas y por inmersión.
- Dejar secar las piezas al aire, sin frotar para no aumentar la carga electrostática que contribuye a que las partículas del aerosol se peguen en las paredes de la cámara.
- Hay que reemplazarlas cuando tengan fisuras.
Ventajas e inconvenientes
Errores en el uso de la cámara inhalatoria
-No agitar el inhalador de cartucho presurizado
-No adaptar bien el inhalador a la cámara.
-No adaptar bien la cámara al rostro o no usar la cámara adecuada a la edad del paciente.
-No realizar un adecuado mantenimiento y limpieza cámara
-No enjuagar la boca
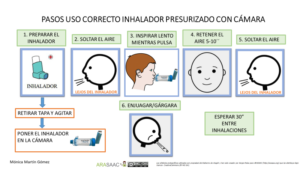
Técnica de uso de la cámara inhalatoria
1- Destapar el inhalador y agitarlo
2- Mantener el inhalador en vertical con la boquilla en la parte inferior.
3-Vaciar los pulmones lentamente, hasta donde sea cómodo
4- Colocar la boquilla, entre los labios y los dientes, evitando que la lengua obstruya la salida de la boquilla. Comenzar a inhalar lentamente, a través de la boca y al mismo tiempo presionar el dispositivo para activar una dosis. (también se puede presionar primero y a continuación inhalar lenta y profundamente)
5-Mantener una inhalación lenta y profunda, a través de la boca, hasta que los pulmones estén llenos de aire.
6-Aguantar la respiración entre 5 y 10 segundos y soplar lentamente (En caso de agudización se puede inhalar y exhalar en cinco ocasiones sin retirar la cámara de la boca y también en menores de 5 años)
7-Cerrar el dispositivo de inhalación
8- Hacer gárgaras y enjuagar la boca al terminar
Imagen 1.- Técnica de uso de cámara de inhalación con presurizado (adultos y niños > 5 años)
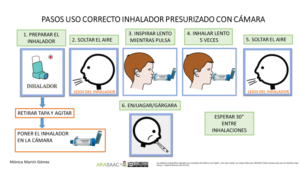
Imagen 2.- Técnica de uso de cámara de inhalación con presurizados niños < 5años
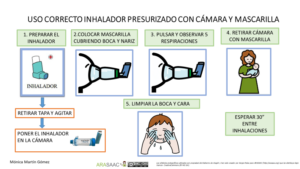
Imagen 3.- Técnica de uso de cámara de inhalación con presurizado en lactantes
En el caso de los lactantes y menores de 5 años que no sepan realizar apnea, se usa una cámara de inhalación con mascarilla del tamaño adecuado para que se adapte a la cara del niño/a.
1.-Se prepara el inhalador previamente: se agita, se retira la tapa y se conecta a la cámara.
2.-Se pulsa solo 1 vez mientras se mantiene la mascarilla en la cara del niño/a cubriendo boca y nariz.
3.-Debe respirar al menos 5 veces (observaremos la válvula de la cámara).
4.-Esperar 30 segundos para nueva inhalación si precisa.
5.- Limpiar la cara y boca del niño/a.
BIBLIOGRAFÍA
- Romero de Ávila G, Gonzálvez Rey J, Mascarós Balaguer E. AGAMFEC. Las 4 reglas de la terapia inhalada [Internet]. Disponible en: https://www.agamfec.com/wp/wp-content/uploads/2015/05/Las4reglasdelaterapiainhalada.pdf
- Plaza V Giner J, Bustamente V, Viejo A, Flor X, Maiz M, et al. GEMA inhaladores. Terapia inhalada: fundamentos, dispositivos y aplicaciones prácticas [internet]. Luzan 5, editor. Madrid; 2018.Disponible en: www.gemasma.com
- Giner J, Plaza V, López-Viña A, Rodrigo G, Neffen H, Casan, P. Consenso SEPAR-ALAT sobre terapia inhalada [internet]. Arch Bronconeumol. 49. 2-14; 2013. Disponible en: http://www.archbronconeumol.org/ el 09/07/2013.
- Gema 5.4. Guía española para el manejo del asma [Internet]. Madrid: Ed. Luzán5; 2024. Disponible en: http://.www.gemasma.com.
- Gema educadores. Manual del educador en asma [Internet]. Madrid: Ed. Luzán5; 2010. Disponible en: http://.www.gemasma.com.
Acreditación de Unidades de Inmunoterapia
A continuación puede encontrar los documentos para guiarle a través del proceso de acreditación de una Unidad de Inmunoterapia:
Guía de Acreditación de Unidades de Inmunoterapia
![]() Guía de acreditación de Unidades de Inmunoterapia(2969 descargas)
Guía de acreditación de Unidades de Inmunoterapia(2969 descargas)
INTRODUCCIÓN
La inmunoterapia es el único tratamiento etiológico de las enfermedades alérgicas mediadas por IgE, mediante la modificación de la respuesta inmunológica. Actualmente, contamos con la administración de inmunoterapia por vía subcutánea, sublingual, intradérmica y en tabletas.
La inmunoterapia no es un tratamiento exento de riesgos inherentes a este, por lo que los pacientes deben ser controlados por personal sanitario adecuadamente formado y siguiendo directrices estrictas que garanticen la seguridad de los pacientes
La frecuencia y gravedad de las reacciones por inmunoterapia dependen de múltiples factores que deben ser evaluados por especialistas en Alergología con experiencia en el manejo de los extractos para inmunoterapia.
Las Unidades de Inmunoterapia (UIT) se encuentran situadas en centro sanitarios (hospitales, centros de especialidades, clínicas privadas…) donde se administra la inmunoterapia específica con alérgenos, sobre todo vía subcutánea, con seguridad y capacidad de evaluación del paciente.
Importancia de las Unidades de Inmunoterapia y metodología de acreditación:
Las UIT deben ser la vanguardia de la administración de los diferentes tipos de extractos, siendo coordinadas por especialistas en Alergología, de forma segura y controlada para los pacientes. Por ello, se hace necesario poner en marcha un procedimiento de acreditación de dichas UIT.
La evaluación de las UIT se basará en el cumplimiento de unos criterios que se clasifican en tres niveles: básicos o imprescindibles, avanzados y de excelencia. Según el grado de cumplimiento de estos criterios, las unidades se acreditarán como UIT avanzada o de excelencia. Para obtener las acreditaciones, debe cumplirse el 100% de los criterios básicos o imprescindibles, y, al menos, el 80% de los criterios avanzados para el nivel avanzado, y el mismo porcentaje de los criterios de excelencia para obtener el nivel de excelencia.
La evaluación de toda la documentación se realizará por miembros seleccionados del Comité de Inmunoterapia conforme al listado de comprobaciones publicado (Anexo 3)
El objetivo de la acreditación es mejorar la atención clínica a los pacientes en tratamiento con inmunoterapia específica con alérgenos, siguiendo criterios de buena práctica clínica. Se trata también de mejorar aún más la seguridad de la administración de este tratamiento y poder implementar el manejo de los datos y su aprovechamiento futuro. Sin duda, estamos convencidos desde el Comité de Inmunoterapia de que el presente sistema de acreditación servirá para unificar criterios, implementar mejoras en cada una de las UIT, así como mejorar la práctica clínica habitual e impulsar la investigación en inmunoterapia específica.
NORMAS Y PROCEMIENTO PARA LA SOLICITUD DE ACREDITACIÓN DE UNIDADES DE INMUNOTERAPIA
- El procedimiento se inicia con la solicitud firmada por el facultativo solicitante y la dirección médica del centro sanitario con los siguientes datos:
- Solicita acreditación: Avanzada o Excelencia
- Nombre del solicitante
- Cargo del solicitante
- Centro de trabajo
- Año de inicio de la Unidad de Inmunoterapia
- Número de pacientes atendidos en la Unidad de Inmunoterapia en el último año
Como normal general, prevalecerá el criterio de veracidad en los datos aportados por el coordinador de la UIT y/o Dirección Médica en los diferentes informes, sin menoscabo de verificaciones o comprobaciones ulteriores por parte de la Comisión de Acreditación de UIT.
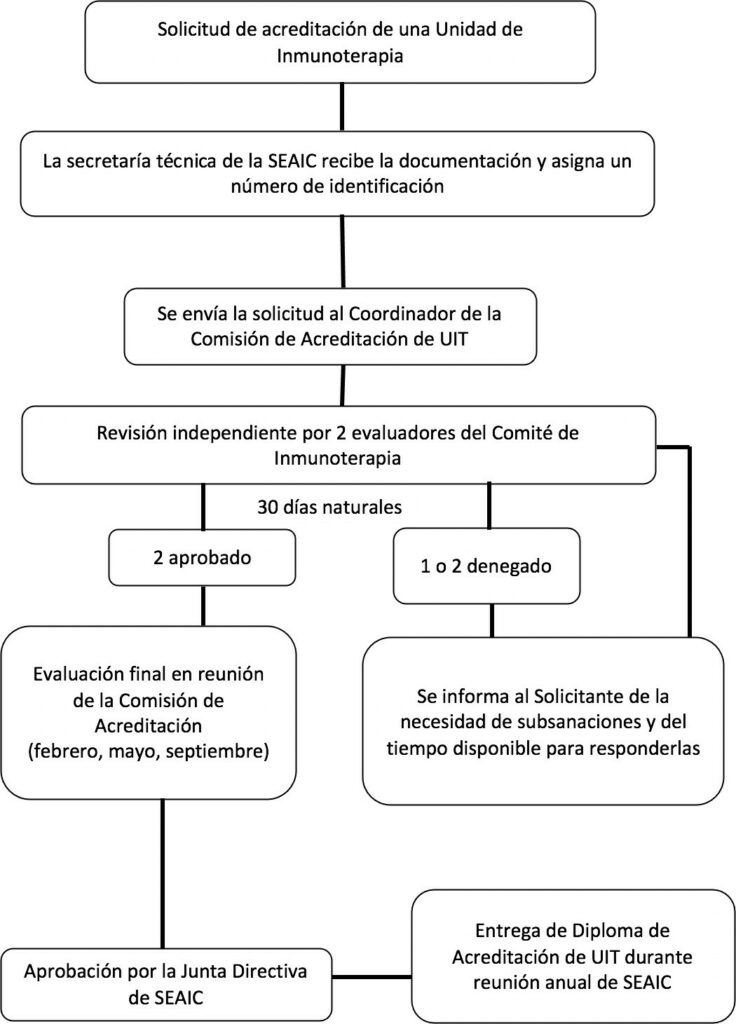
- Las solicitudes de acreditación y los documentos adjuntos del centro solicitante serán recibidas por la Secretaría Técnica de la Sociedad Española de Alergología e Inmunología Clínica (SEAIC) que confirmará la recepción de la documentación al solicitante por correo electrónico.
- La Secretaría Técnica de la SEAIC comprobará que se ha recibido toda la documentación requerida y asignará un número de identificación único para cada solicitud. A través de un correo electrónico, confirmará al solicitante la recepción, el número de identificación asignado a la solicitud y se informará de que la solicitud pasa a trámite de evaluación.
- La Secretaría Técnica de la SEAIC enviará la solicitud al Coordinador de la Comisión de Acreditación de UIT, que procederá a la asignación de los evaluadores.
- Cada solicitud es valorada por dos evaluadores del Comité de Inmunoterapia que revisan los documentos e informes de forma Los evaluadores cuentan con un plazo de 30 días naturales para emitir el resultado de la evaluación al Coordinador de la Comisión de Acreditación de UIT.
- Se puede solicitar la acreditación de UIT de nivel AVANZADO y nivel EXCELENTE. Para obtener la acreditación todas las UIT deben cumplir un 100% de los criterios básicos o imprescindibles y:
- al menos el 80% de los criterios avanzados para la acreditación de UIT Avanzada.
- al menos un 80% de los criterios de excelencia para la acreditación de UIT de
- El resultado puede se “aprobada” en el caso de que se cumpla el porcentaje necesario de los requisitos para la acreditación solicitada; o “denegada” en el caso de no se cumpla.
- En caso de que uno o ambos evaluadores emitan una valoración negativa, se comunicarán al solicitante las subsanaciones que debe realizar mediante correo electrónico.
- Cuando se reciba la contestación a las subsanaciones, estas serán evaluadas de nuevo por los revisores, siguiendo el mismo proceso descrito anteriormente.
- Cuando el dictamen de ambos evaluadores sea favorable, la solicitud pasará a ser evaluada en la siguiente reunión de la Comisión de Acreditación para la aprobación final de la acreditación de la La Comisión de Acreditación celebra tres reuniones anuales (febrero, mayo y septiembre).
- Tras la aprobación de la acreditación de la UIT por la Comisión de Acreditación, la solicitud será presentada a la Junta Directiva de la SEAIC que otorgará la aprobación
- El solicitante recibirá notificación de la concesión de acreditación en los siguientes 15 días hábiles tras la aprobación definitiva por la Junta Directiva de la SEAIC.
- Las UIT acreditadas recibirán el Diploma de Acreditación durante la reunión nacional anual de la SEAIC.
- Las UIT acreditadas deberán re-acreditarse cada 5 años.
¿CÓMO TRAMITAR SU SOLICITUD?
1) PREPARE SU SOLICITUD
1.1) VERIFIQUE QUE SU UNIDAD DE IT CUMPLA CON LOS CRITERIOS BÁSICOS DE ACREDITACIÓN Y VALORE EL TIPO DE SOLICITUD QUE QUIERE PRESENTAR.
Descargue el listado de criterios para la acreditación (Anexo I)
1.2) RECOJA LA DOCUMENTACIÓN QUE TIENE QUE REMITIR JUNTO CON SU SOLICITUD. Rogamos
que nombre los archivos o anexos de manera clara para facilitar su clasificación. (por ejemplo: Doc1 Informe jefe, Doc2 CV etc. Es aconsejable que incluya una lista con la relación de documentos remitidos).
Descargue la lista de documentación requerida para la acreditación (Anexo II)
Descargue la lista de verificación (Anexo III checklist)
2) PRESENTE SU SOLICITUD DE MANERA TELEMÁTICA
2.1) SELECCIONE EL TIPO DE ACREDITACIÓN QUE QUIERE SOLICITAR y pinche en el enlace
correspondiente. COMPLETE EL FORMULARIO ONLINE.
ACCESO A SOLICITUD ONLINE de UIT AVANZADA
ACCESO A SOLICITUD ONLINE UIT DE EXCELENCIA
IMPORTANTE: el formulario de solicitud debe cumplimentarse todo de una vez. No permite que se pueda guardar en borrador. Sin embargo, sí permite volver a editarlo una vez que se ha enviado es decir que mediante un enlace podrá hacer alguna corrección si hubiera cometido algún error.
2.2) ENVÍE TODA LA DOCUMENTACIÓN NECESARIA PARA SU SOLICITUD.
Dirección de envío: uit@seaic.org
ANEXO I Listado de criterios para la acreditación de Unidades de Inmunoterapia
![]() Anexo 1: Listado de criterios para la acreditación de Unidades de Inmunoterapia(2909 descargas)
Anexo 1: Listado de criterios para la acreditación de Unidades de Inmunoterapia(2909 descargas)
CRITERIOS BÁSICOS (IMPRESCINDIBLES)
1. Un alergólogo o enfermera con acceso al alergólogo.
2. Un alergólogo o enfermera disponible (por cercanía y acceso) tras la administración del
tratamiento para responder cuestiones durante aproximadamente 10-20 minutos por paciente y dosis administrada.
3. Una enfermera accesible rápidamente (por cercanía y acceso) para responder preguntas incluso en caso de que el alergólogo no esté disponible.
4. Consulta médica específica, o un área de enfermería específica, como un área de consulta para exploración y evaluación de pacientes (estos espacios podrían compartirse con otras actividades).
5. Área que permita la observación del paciente después del tratamiento durante al menos 30 minutos.
6. Área de espera (sillas para los pacientes y niños, o dependientes).
7. Una camilla, escritorio para el médico, armarios para el almacenamiento de suministros y neveras si se almacenan extractos.
8. Medicación parenteral: adrenalina, antihistamínicos, corticosteroides, broncodilatadores, y dispositivos para su administración.
9. Medicación oral: antihistamínicos, corticosteroides.
10. Medicamentos inhalados: broncodilatadores de acción rápida.
11. Oxígeno y dispositivos para administrarlo.
12. Nebulizadores y cámaras de inhalación.
13. Jeringuillas de 1 ml con agujas subcutáneas, jeringas para inyección intramuscular, sistemas de perfusión, fluidos, algodón / gasa, antisépticos (clorhexidina o alcohol), torniquetes y temporizadores.
14. Instrumentos para monitorizar signos vitales (frecuencia cardíaca, presión arterial, pulsioximetría), pico flujo máximo, espirómetro, fonendoscopio.
15. El teléfono como canal de comunicación y de alerta a urgencias.
16. Protocolo de administración para inmunoterapia específica (ITE).
17. Protocolo de acción en caso de reacciones adversas.
18. Monitorización de la tolerancia.
19. Coordinación con Atención Primaria en caso de que se remita a Atención Primaria.
20. Registro de las administraciones e incidencias del paciente.
21. Canal de comunicación con Primaria (si es posible a través de informes) que permita la coordinación entre Atención Primaria y Atención Especializada si los pacientes son derivados a Atención Primaria.
22. Registro y notificación de reacciones adversas (por lo menos en el caso de reacciones graves) a las autoridades de farmacovigilancia.
CRITERIOS AVANZADOS
1. Un alergólogo con dedicación no exclusiva.
2. Una enfermera entrenada en la administración de extractos.
3. Área de enfermería para la preparación de la dosis de ITE, con zona de almacenamiento y neveras para la medicación.
4. Área para administración de ITE con la posibilidad de tratamiento simultáneo de varios pacientes.
5. Área de atención urgente con todo el material necesario para el tratamiento de las reacciones adversas y línea telefónica directa con UCI.
6. Base de datos clínica informatizada de pacientes a la que pueden acceder todos los miembros de la unidad.
7. Capacidad para administrar ITE subcutánea.
8. Capacidad para iniciar cualquier ITE sublingual.
9. Capacidad de explicar al paciente y educarlo en el uso posterior de la ITE sublingual (incluyendo la posibilidad de reacciones en el domicilio).
10. Capacidad para administrar la primera dosis de cualquier ITE que no sea experimental o que tenga ficha técnica.
11. Capacidad para administrar ITE para aeroalérgenos.
12. Capacidad para realizar ITE con veneno de himenópteros.13. Capacidad para administrar cualquier extracto comercial, ya probado, independientemente del riesgo asociado.
14. Capacidad para administrar extractos nativos y modificados.
15. Capacidad para administrar extractos acuosos.
16. Capacidad para administrar pautas de inicio convencionales o agrupadas y mantenimientos en pacientes con reacciones previas.
17. Proporcionar de forma sistemática, oral o escrita información de la ITE (indicaciones, contraindicaciones, coste, objetivos, riesgos y beneficios esperados) en todos los pacientes.
18. Disponibilidad de un documento con instrucciones individualizadas que contenga toda la información relacionada con la ITE, accesible cuando se administre cada dosis.
19. Completar el documento de instrucciones individualizado al menos el 80% de las veces.
20. Disponer de una lista de verificación de administración de ITE que incluya todas las variables que deben ser comprobadas antes de administrar cada dosis.
21. Utilizar la lista de verificación en al menos el 60% de los casos.
22. Monitorización de la seguridad y eficacia.
23. Suministrar información a los pacientes del almacenamiento de extractos, cuando sean ellos quienes los guarden.
24. Existencia de un Plan de Seguridad del paciente que especifique como responder ante reacciones tanto inmediatas como retardadas con personal entrenado y los recursos necesarios para dicha respuesta.
25. Existencia de un registro de reacciones sistémicas inmediatas y tardías donde se registren el 100% de las reacciones acontecidas.
26. Existencia de un Plan de Seguridad que incluya adrenalina y sueros.
27. Existencia de un registro de la administración de medicación para reacciones inmediatas.
28. Aplicación en la unidad de un protocolo preexistente de anafilaxia.
29. Adaptación de los procedimientos estándar a niños, en el caso de que se atiendan menores.
30. Disponibilidad de un documento escrito acordado con Atención Primaria para la administración de ITE.
31. Recogida y clasificación de todas las reacciones adversas conforme a las guías.
32. Disponibilidad de una línea de comunicación durante las horas de servicio o bien de forma continuada (según la capacidad) para resolver las incidencias.
33. Registro de las incidencias tras administración de ITE en la historia clínica en el 60-80% de los casos.
34. Realización de un curso de RCP básica cada 2 años y de RCP avanzada cada 5 años, por le personal médico de la unidad.
35. Realización de un curso de RCP básica por el personal de enfermería de la unidad cada 2 años.
36. Organización de sesiones con problemas clínicos en la unidad de ITE.
CRITERIOS PARA LA EXCELENCIA
1. Al menos 2 alergólogos con dedicación no exclusiva.
2. Área de observación en el área de administración de ITE o cerca de ella con capacidad dobservación al paciente durante más de 4 horas.
3. Área de atención urgente con todos los materiales necesarios para el tratamiento de reacciones adversas, que permita el inicio de maniobras de RCP con proximidad a la UCI, y una línea telefónica para llamar a la UCI.
4. Disponibilidad del siguiente material para el diagnóstico y tratamiento de reacciones adversas: 1-Carro de reanimación completo (con desfibrilador y todos los suministros y medicamentos necesarios para responder al paro cardiorrespiratorio).
2. Monitor de constantes vitales.
5. Posibilidad de utilizar datos del registro médico de pacientes a través de ordenador accesible para todos los miembros de la unidad.
6. Posibilidad de usar extractos experimentales (en investigación, no comercializados).
7. Posibilidad de administrar ITE en pacientes de alto riesgo (ej. mastocitosis, reacciones sistémicas previas).
8. Completar el documento de instrucciones individualizado al menos el 90% de las veces.
9. Disponibilidad de una lista de verificación para la administración de ITE de acuerdo con el nivel de pacientes que pueden ser tratados (alto riesgo) con variables específicas.
10. Completar la lista de comprobación en al menos el 90% de los casos.
11. Posibilidad de acceder a los datos de forma informática para recoger las dosis administradas.
12. Monitorizar la eficacia y seguridad usando unos parámetros objetivos
13. Aplicar medidas de control de almacenamiento del extracto (termómetro) y garantizara la conservación a la temperatura correcta.
14. Disponer de un plan de seguridad que incluya la monitorización.
15. Disponibilidad de un cuestionario de satisfacción del paciente.
16. Calendario específico para ITE que incluya huecos para consultas urgentes de los pacientes sin cita.
17. Disponibilidad de documento detallado o registro con todos los datos relacionados con la ITE, que incluya información sobre el extracto, la dosis, tolerabilidad, fecha de inicio, medidas del PEF.
18. Respuesta a incidencias relacionadas con ITE en 48-72 horas.
19. Registro de incidentes en más del 80% de los casos.
20. Acreditación de formación médica continuada en Inmunoterapia, del personal médico de la unidad de ITE.
21. Formar parte como miembro en una red específica de ITE o participación en algún proyecto de IT específica en los últimos 5 años.
22. Sistema de auditoría interna para evaluar la recogida de reacciones adversas.
23. Implementación del ciclo PDCA para la mejoría continuada.
24. Miembros pertenecientes a sociedades científicas.
BAREMOS PARA LA ADJUDICACIÓN:
IMPRESCINDIBLES (DEBEN CUMPLIRSE EL 100%. 22/22) AVANZADOS (DEBEN CUMPLIRSE 80%. 29/36) EXCELENCIA (DEBEN CUMPLIRSE 80%. 20/25)
ANEXO II Listado de documentos requeridos
A continuación, se detalla la documentación que se debe de presentar para optar por la acreditación de una Unidad de Inmunoterapia (UIT).
La evaluación de las UIT de basará en el cumplimiento de unos criterios que se clasifican en tres niveles: básicos o imprescindibles, avanzados y de excelencia. Según el grado de cumplimiento de estos criterios, las unidades se acreditarán como avanzada o de excelencia.
Se puede solicitar la acreditación de UIT de nivel AVANZADO y nivel EXCELENTE.
Para obtener la acreditación todas las UIT deben cumplir un 100% de los criterios básicos o imprescindibles y
- al menos el 80% de los criterios avanzados para la acreditación de UIT
- al menos un 80% de los criterios de excelencia para la acreditación de UIT de Excelencia.
Todos los criterios que se detallan a continuación deben aparecer reflejados en el informe que acompañe a la solicitud, en los casos señalados se deberán adjuntar además los documentos especificados que justifiquen su existencia.
| Criterio | Modo de Evaluación | Tipo de criterio Deben cumplirse 100% |
| Un alergólogo o enfermera con acceso al alergólogo | Informe del responsable de la Unidad de Inmunoterapia. Curriculum vitae. | IMPRESCINDIBLE |
| Un alergólogo o enfermera con acceso al alergólogo para responder preguntas tras la administración del tratamiento | Informe del responsable de la Unidad de Inmunoterapia y plano de situación |
IMPRESCINDIBLE |
| Enfermera accesible rápidamente (por cercanía y acceso) para responder preguntas incluso en caso de que el alergólogo no esté disponible | Informe del responsable de la Unidad de Inmunoterapia y plano |
IMPRESCINDIBLE |
| Consulta médica específica, o un área de enfermería específica, como un área de consulta para exploración y evaluación de pacientes (estos espacios podrían |
Fotos y/o plano |
IMPRESCINDIBLE |
| compartirse con otras actividades). | ||
| Área que permita la observación del paciente después del tratamiento durante al menos 30 minutos |
Fotos y/o plano |
IMPRESCINDIBLE |
| Área de espera (sillas para los pacientes y niños, o dependientes) | Fotos y/o plano | IMPRESCINDIBLE |
| Una camilla, escritorio para el médico, armarios para el almacenamiento de suministros y neveras si se almacenan extractos | Informe del responsable de la Unidad de Inmunoterapia |
IMPRESCINDIBLE |
| Medicación parenteral: adrenalina, antihistamínicos, corticosteroides, broncodilatadores, y dispositivos para su administración. |
Informe del responsable de la Unidad de Inmunoterapia |
IMPRESCINDIBLE |
| Medicación oral: antihistamínicos, corticosteroides | Informe del responsable de la Unidad de Inmunoterapia | IMPRESCINDIBLE |
| Medicamentos inhalados: broncodilatadores de acción rápida | Informe del responsable de la Unidad de Inmunoterapia | IMPRESCINDIBLE |
| Oxígeno y dispositivos para administrarlo | Informe del responsable de la Unidad de Inmunoterapia | IMPRESCINDIBLE |
| Nebulizadores y cámaras de inhalación | Informe del responsable de la Unidad de Inmunoterapia | IMPRESCINDIBLE |
| Jeringuillas de 1 ml con agujas subcutáneas, jeringas para inyección intramuscular, sistemas de perfusión, fluidos, algodón / gasa, antisépticos (clorhexidina o alcohol), torniquetes y temporizadores |
Informe del responsable de la Unidad de Inmunoterapia |
IMPRESCINDIBLE |
| Instrumentos para monitorizar signos vitales (frecuencia cardíaca, presión arterial, pulsioximetría), pico flujo | Informe del responsable de la Unidad de Inmunoterapia | IMPRESCINDIBLE |
| máximo, espirómetro, fonendoscopio | ||
| El teléfono como canal de comunicación y de alerta a urgencias | Informe del responsable de la Unidad de Inmunoterapia | IMPRESCINDIBLE |
| Protocolo de administración de inmunoterapia específica (ITE) | Informe y Documento con la descripción del procedimiento, pautas y medidas de seguridad | IMPRESCINDIBLE |
| Protocolo de acción en caso de reacciones adversas | Informe y Documento con la descripción del procedimiento de actuación ante reacciones adversas | IMPRESCINDIBLE |
| Monitorización de la tolerancia | Informe del responsable de la Unidad de Inmunoterapia | IMPRESCINDIBLE |
| Coordinación con Atención Primaria en caso de que se remita a Atención Primaria | Informe y Documento informativo para AP a modo de guía de administración de las dosis, técnica de administración de las diferentes IT y ajuste de dosis en caso de retraso de administración. |
IMPRESCINDIBLE |
| Registro de las administraciones e incidencias del paciente | Informe que detalle cómo se registran y almacenan esos datos. | IMPRESCINDIBLE |
| Canal de comunicación con Primaria (si es posible a través de informes) que permita la coordinación entre Atención Primaria y Atención Especializada si los pacientes son derivados a Atención Primaria |
Informe del responsable de la Unidad de Inmunoterapia |
IMPRESCINDIBLE |
| Registro y notificación de reacciones adversas (por lo menos en el caso de reacciones graves) a las autoridades de farmacovigilancia |
Informe del responsable de la Unidad de Inmunoterapia |
IMPRESCINDIBLE |
| Criterio | Modo de Evaluación | Tipo de criterio Deben cumplirse 80% (29/36) |
| Un alergólogo con dedicación no exclusiva | Informe del responsable de la Unidad de Inmunoterapia. Curriculum vitae | AVANZADO |
| Enfermera entrenada en la administración de extractos | Informe del responsable de la Unidad de Inmunoterapia y Curriculum vitae | AVANZADO |
| Área de enfermería para la preparación de la dosis de ITE, con zona de almacenamiento y neveras para la medicación |
Fotos y/o plano |
AVANZADO |
| Área para administración de ITE con la posibilidad de tratamiento simultáneo de varios pacientes | Fotos y/o plano (el área de observación y espera puede ser la misma. No puede ser el despacho del facultativo) |
AVANZADO |
| Área de atención urgente con todo el material necesario para el tratamiento de las reacciones adversas y línea telefónica directa con UCI | Informe del responsable de la Unidad de Inmunoterapia |
AVANZADO |
| Base de datos clínica informatizada de pacientes a la que pueden acceder todos los miembros de la unidad. | Informe del responsable de la Unidad de Inmunoterapia |
AVANZADO |
| Capacidad para administrar ITE subcutánea | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Capacidad para iniciar cualquier ITE sublingual. | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Capacidad de explicar al paciente y educarlo en el uso posterior de la ITE sublingual (incluyendo la posibilidad de reacciones en el domicilio). | Informe y Certificado de buenas prácticas clínicas |
AVANZADO |
| Capacidad para administrar la primera dosis de cualquier ITE que no sea experimental o que tenga ficha técnica | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Capacidad para administrar ITE para aeroalérgenos | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Capacidad para realizar ITE con veneno de himenópteros | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Capacidad para administrar cualquier extracto comercial, ya probado, independientemente del riesgo asociado | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Capacidad para administrar extractos nativos y modificados | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Capacidad para administrar extractos acuosos | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Capacidad para administrar pautas de inicio convencionales o agrupadas y mantenimientos en pacientes con reacciones previas | Informe del responsable de la Unidad de Inmunoterapia |
AVANZADO |
| Proporcionar de forma sistemática, oral o escrita información de la ITE (indicaciones, contraindicaciones, coste, objetivos, riesgos y beneficios esperados) en todos los pacientes. |
Informe del responsable de la Unidad de Inmunoterapia y Documento |
AVANZADO |
| Disponibilidad de un documento con instrucciones individualizadas que contenga toda la información relacionada con la ITE, accesible cuando se administre cada dosis |
Informe del responsable de la Unidad de Inmunoterapia y Documento |
AVANZADO |
| Completar el documento de instrucciones individualizado al menos el 80% de las veces. | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Disponer de una lista de verificación de administración de ITE que incluya todas las variables que deben ser comprobadas | Informe y Documento con la lista de verificación de variables a comprobar antes de cada administración | AVANZADO |
| antes de administrar cada dosis. | ||
| Utilizar la lista de verificación en al menos el 60% de los casos | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Monitorización de la seguridad y eficacia | Descripción | AVANZADO |
| Suministrar información a los pacientes del almacenamiento de extractos, cuando sean ellos quienes los guarden | Informe del responsable de la Unidad de Inmunoterapia |
AVANZADO |
| Existencia de un Plan de Seguridad del paciente que especifique como responder ante reacciones tanto inmediatas como retardadas con personal entrenado y los recursos necesarios para dicha respuesta. |
Documento Cartilla de Inmunoterapia |
AVANZADO |
| Existencia de un registro de reacciones sistémicas inmediatas y tardías donde se registren el 100% de las reacciones acontecidas | Informe del responsable de la Unidad de Inmunoterapia y Documento | AVANZADO |
| Existencia de un Plan de Seguridad que incluya adrenalina y sueros | Informe y Documento con la descripción del procedimiento de actuación ante reacciones adversas | AVANZADO |
| Existencia de un registro de la administración de medicación para reacciones inmediatas | Informe (listado de la medicación disponible en la UIT) | AVANZADO |
| Aplicación en la unidad de un protocolo preexistente de anafilaxia | Informe y Protocolo de manejo de anafilaxia | AVANZADO |
| Adaptación de los procedimientos estándar a niños, en el caso de que se atiendan menores | Informe y Documento con descripción de las dosis ajustadas para población pediátrica | AVANZADO |
| Disponibilidad de un documento escrito acordado con Atención Primaria para la administración de ITE | Informe del responsable de la Unidad de Inmunoterapia y Documento |
AVANZADO |
| Recogida y clasificación de todas las reacciones adversas conforme a las guías | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Disponibilidad de una línea de comunicación durante las horas de servicio o bien de forma continuada (según la capacidad) para resolver las incidencias |
Informe del responsable de la Unidad de Inmunoterapia |
AVANZADO |
| Registro de las incidencias tras administración de ITE en la historia clínica en el 60-80% de los casos | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Realización de un curso de RCP básica cada 2 años y de RCP avanzada cada 5 años, por el personal médico de la unidad | Certificado o diploma de al menos un facultativo responsable de la UIT |
AVANZADO |
| Realización de un curso de RCP básica por el personal de enfermería de la unidad cada 2 años | Certificado o diploma de al menos un responsable de enfermería de la UIT | AVANZADO |
| Organización de sesiones con problemas clínicos en la unidad de ITE | Informe del responsable de la Unidad de Inmunoterapia | AVANZADO |
| Criterio | Modo de Evaluación | Tipo de criterio Deben cumplirse 80% (20/24) |
| Al menos 2 alergólogos con dedicación no exclusiva. | Informe del responsable de la Unidad de Inmunoterapia y de la Dirección Médica | EXCELENCIA |
| Área de observación en el área de administración de ITE o cerca de ella con capacidad de observación al paciente durante más de 4 horas. | Informe del responsable de la Unidad de Inmunoterapia y de la Dirección Médica |
EXCELENCIA |
| Área de atención urgente con todos los materiales necesarios para el tratamiento de reacciones adversas, que permita el inicio de maniobras de RCP con proximidad a la UCI, y una línea telefónica para llamar a la UCI. |
Informe del responsable de la Unidad de Inmunoterapia y de la Dirección Médica |
EXCELENCIA |
| Disponibilidad del siguiente material para el diagnóstico y tratamiento de reacciones adversas: 1. Carro de reanimación completo (con desfibrilador y todos los suministros y medicamentos necesarios para responder al paro cardiorrespiratorio). 2. Monitor de constantes vitales. |
Fotos |
EXCELENCIA |
| Posibilidad de utilizar datos del registro médico de pacientes a través de ordenador accesible para todos los miembros de la unidad. | Informe con la descripción informática de la explotación de la base de datos |
EXCELENCIA |
| Posibilidad de usar extractos experimentales (en investigación, no comercializados). | Informe del responsable de la Unidad de Inmunoterapia y de la Dirección Médica | EXCELENCIA |
| Posibilidad de administrar ITE en pacientes de alto riesgo (ej. mastocitosis, | Informe del responsable de la Unidad de Inmunoterapia | EXCELENCIA |
| reacciones sistémicas previas). | ||
| Completar el documento de instrucciones individualizado al menos en el 90% de las veces. | Informe del responsable de la Unidad de Inmunoterapia | EXCELENCIA |
| Disponibilidad de una lista de verificación para la administración de ITE de acuerdo con el nivel de pacientes que pueden ser tratados (alto riesgo) con variables específicas. | Informe del responsable de la Unidad de Inmunoterapia Incluir el documento con el listado de comprobación |
EXCELENCIA |
| Completar la lista de verificación en al menos el 90% de los casos | Informe del responsable de la Unidad de Inmunoterapia | EXCELENCIA |
| Posibilidad de acceder a los datos de forma informática para recoger las dosis administradas. | Informe con la descripción de la metodología de explotación de estos datos | EXCELENCIA |
| Monitorizar la eficacia y seguridad usando unos parámetros objetivos. | Informe detallando la práctica habitual (valoración de la reacción local, registro PF, clasificación EACCI de las reacciones etc…) | EXCELENCIA |
| Aplicar medidas de control de almacenamiento del extracto (termómetro) y garantizara la conservación a la temperatura correcta. | Informe del responsable de la Unidad de Inmunoterapia |
EXCELENCIA |
| Disponer de un plan de seguridad que incluya la monitorización. | Informe y Documento interno para resolución de contingencias en seguridad y monitorización de estas situaciones |
EXCELENCIA |
| Disponibilidad de un cuestionario de satisfacción del paciente. | Informe del responsable de la Unidad de Inmunoterapia y Documento | EXCELENCIA |
| Calendario específico para ITE que incluya huecos para consultas urgentes de los pacientes sin cita. | Informe del responsable de la Unidad de Inmunoterapia | EXCELENCIA |
| Disponibilidad de documento detallado o registro con todos los datos relacionados con la ITE, que incluya información sobre el | Informe del responsable de la Unidad de Inmunoterapia y Documento |
EXCELENCIA |
| extracto, la dosis, tolerabilidad, fecha de inicio, medidas del pico flujo espiratorio. | ||
| Respuesta a incidencias relacionadas con ITE en 48- 72 horas. | Informe del responsable de la Unidad de Inmunoterapia | EXCELENCIA |
| Registro de incidentes en más del 80% de los casos. | Informe del responsable de la Unidad de Inmunoterapia | EXCELENCIA |
| Acreditación de formación médica continuada en Inmunoterapia, del personal médico de la unidad de IT. | Certificados DPC Cursos acreditados en IT | EXCELENCIA |
| Formar parte como miembro en una red específica de IT o participación en algún proyecto de IT específica en los últimos 5 años. | Documentos o publicaciones que acrediten la participación en estudios/ensayos clínicos con inmunoterapia |
EXCELENCIA |
| Sistema de auditoría interna para evaluar la recogida de reacciones adversas. | Informe del responsable de la Unidad de Inmunoterapia | EXCELENCIA |
| Implementación del ciclo PDCA para la mejoría continuada. | Documento con aspectos específicos a mejorar y cómo se van a implementar esos cambios | EXCELENCIA |
| Miembros pertenecientes a sociedades científicas. | Certificados | EXCELENCIA |
ANEXO III Checklist de criterios para la acreditación de Unidades de Inmunoterapia
![]() Anexo 3: Checklist de criterios de acreditacion de Unidades Inmunoterapia(1987 descargas)
Anexo 3: Checklist de criterios de acreditacion de Unidades Inmunoterapia(1987 descargas)
IMPRESCINDIBLES (IM) - AVANZADOS (AV) - EXCELENCIA (EX)
Documentación que se debe aportar para solicitar la acreditación. Se adjuntará junto con los informes o documentos que se detallan en el modo de evaluación.
| Criterios IMPRESCINDIBLES | Modo evaluación | Tipo | check |
| 1. Un alergólogo o enfermera con acceso al alergólogo. | Informe y CV | IM | ☐ |
| 2. Un alergólogo o enfermera con acceso al alergólogo para responder preguntas. | Informe y plano | IM | ☐ |
| 3. Enfermera accesible rápidamente (por cercanía y acceso) para responder preguntas incluso en caso de que el alergólogo no esté disponible. | Informe y plano | IM | ☐ |
| 4. Consulta médica específica, o un área de enfermería específica, como un área de consulta para exploración y evaluación de pacientes (estos espacios podrían compartirse con otras actividades). | Fotos y/o plano | IM | ☐ |
| 5. Área que permita la observación del paciente después del tratamiento durante al menos 30 minutos | Fotos y/o plano | IM | ☐ |
| 6. Área de espera (sillas para los pacientes y niños, o dependientes). | Fotos y/o plano | IM | ☐ |
| 7. Una camilla, escritorio para el médico, armarios para el almacenamiento de suministros y neveras si se almacenan extractos. | Informe | IM | ☐ |
| 8. Medicación parenteral: adrenalina, antihistamínicos, corticosteroides, broncodilatadores, y dispositivos para su administración. | Informe | IM | ☐ |
| 9. Medicación oral: antihistamínicos, corticosteroides. | Informe | IM | ☐ |
| 10. Medicamentos inhalados: broncodilatadores de acción rápida. | Informe | IM | ☐ |
| 11. Oxígeno y dispositivos para administrarlo. | Informe | IM | ☐ |
| 12. Nebulizadores y cámaras de inhalación. | Informe | IM | ☐ |
| 13. Jeringuillas de 1 ml con agujas subcutáneas, jeringas para inyección intramuscular, sistemas de perfusión, fluidos, algodón / gasa, antisépticos (clorhexidina o alcohol), torniquetes y temporizadores. | Informe | IM | ☐ |
| 14. Instrumentos para monitorizar signos vitales (FC, presión arterial, pulsioximetría), pico flujo máximo, espirómetro, fonendoscopio. | Informe | IM | ☐ |
| 15. El teléfono como canal de comunicación y de alerta a urgencias. | Informe | IM | ☐ |
| 16. Protocolo de administración para inmunoterapia específica (ITE). | Informe y documento | IM | ☐ |
| 17. Protocolo de acción en caso de reacciones adversas. | Informe y documento | IM | ☐ |
| 18. Monitorización de la tolerancia. | Informe | IM | ☐ |
| 19. Coordinación con Atención Primaria en caso de que se remita a Atención Primaria. | Informe y documento | IM | ☐ |
| 20. Registro de las administraciones e incidencias del paciente. | Informe | IM | ☐ |
| 21. Canal de comunicación con Primaria (si es posible a través de informes) que permita la coordinación entre Atención Primaria y Atención Especializada si los pacientes son derivados a Atención Primaria. | Informe | IM | ☐ |
| 22. Registro y notificación de reacciones adversas (por lo menos en el caso de reacciones graves) a las autoridades de farmacovigilancia. | Informe | IM | ☐ |
| Criterios AVANZADOS | Modo evaluación | Tipo | check |
| 1. Un alergólogo con dedicación no exclusiva. | Informe y CV | AV | ☐ |
| 2. Enfermera entrenada en la administración de extractos. | Informe y CV | AV | ☐ |
| 3. Área de enfermería para la preparación de la dosis de ITE, con zona de almacenamiento y neveras para la medicación. | Fotos y/o planos | AV | ☐ |
| 4. Área para administración de ITE con la posibilidad de tratamiento simultáneo de varios pacientes. | Fotos/planos | AV | ☐ |
| 5. Área de atención urgente con todo el material necesario para el tratamiento de las reacciones adversas y línea telefónica directa con UCI. | Informe | AV | ☐ |
| 6. Base de datos clínica informatizada de pacientes a la que pueden acceder todos los miembros de la unidad. | Informe | AV | ☐ |
| 7. Capacidad para administrar ITE subcutánea. | Informe | AV | ☐ |
| 8. Capacidad para iniciar cualquier ITE sublingual. | Informe | AV | ☐ |
| 9. Capacidad de explicar al paciente y educarlo en el uso posterior de la ITE sublingual (incluyendo la posibilidad de reacciones en el domicilio). | Informe. Certificado de BPC | AV | ☐ |
| 10. Capacidad para administrar la primera dosis de cualquier ITE que no sea experimental o que tenga ficha técnica | Informe | AV | ☐ |
| 11. Capacidad para administrar ITE para aeroalérgenos. | Informe | AV | ☐ |
| 12. Capacidad para realizar ITE con veneno de himenópteros. | Informe | AV | ☐ |
| 13. Capacidad para administrar cualquier extracto comercial, ya probado, independientemente del riesgo asociado. | Informe | AV | ☐ |
| 14. Capacidad para administrar extractos nativos y modificados. | Informe | AV | ☐ |
| 15. Capacidad para administrar extractos acuosos. | Informe | AV | ☐ |
| 16. Capacidad para administrar pautas de inicio convencionales o agrupadas y mantenimientos en pacientes con reacciones previas. | Informe | AV | ☐ |
| 17. Proporcionar de forma sistemática, oral o escrita información de la ITE (indicaciones, contraindicaciones, coste, objetivos, riesgos y beneficios esperados) en todos los pacientes. | Informe y Documento | AV | ☐ |
| 18. Disponibilidad de un documento con instrucciones individualizadas que contenga toda la información relacionada con la ITE, accesible cuando se administre cada dosis. | Informe y Documento | AV | ☐ |
| 19. Completar el documento de instrucciones individualizado al menos el 80% de las veces. | Informe | AV | ☐ |
| 20. Disponer de una lista de verificación de administración de ITE que incluya todas las variables que deben ser comprobadas antes de administrar cada dosis. | Informe y Documento | AV | ☐ |
| 21. Utilizar la lista de verificación en al menos el 60% de los casos. | Informe | AV | ☐ |
| 22. Monitorización de la seguridad y eficacia. | Descripción | AV | ☐ |
| 23. Suministrar información a los pacientes del almacenamiento de extractos, cuando sean ellos quienes los guarden. | Informe | AV | ☐ |
| 24. Existencia de un Plan de Seguridad del paciente que especifique como responder ante reacciones tanto inmediatas como retardadas con personal entrenado y los recursos necesarios para dicha respuesta. | Cartilla Inmunoterap ia | AV | ☐ |
| 25. Existencia de un registro de reacciones sistémicas inmediatas y tardías donde se registren el 100% de las reacciones acontecidas. | Informe y Documento | AV | ☐ |
| 26. Existencia de un Plan de Seguridad que incluya adrenalina y sueros | Informe y Documento | AV | ☐ |
| 27. Existencia de un registro de la administración de medicación para reacciones inmediatas. | Informe | AV | ☐ |
| 28. Aplicación en la unidad de un protocolo preexistente de anafilaxia. | Informe y Protocolo | AV | ☐ |
| 29. Adaptación de los procedimientos estándar a niños, en el caso de que se atiendan menores. | Informe y Documento | AV | ☐ |
| 30. Disponibilidad de un documento escrito acordado con Atención Primaria para la administración de ITE. | Informe y Documento | AV | ☐ |
| 31. Recogida y clasificación de todas las reacciones adversas conforme a las guías. | Informe | AV | ☐ |
| 32. Disponibilidad de una línea de comunicación durante las horas de servicio o bien de forma continuada (según la capacidad) para resolver las incidencias. | Informe | AV | ☐ |
| 33. Registro de las incidencias tras administración de ITE en la historia clínica en el 60-80% de los casos. | Informe | AV | ☐ |
| 34. Realización de un curso de RCP básica cada 2 años y de RCP avanzada cada 5 años, por el personal médico de la unidad. | Certificado o diploma | AV | ☐ |
| 35. Realización de un curso de RCP básica por el personal de enfermería de la unidad cada 2 años. | Certificado o diploma | AV | ☐ |
| 36. Organización de sesiones con problemas clínicos en la unidad de ITE. | Informe | AV | ☐ |
| Criterios EXCELENCIA | Modo evaluación | Tipo | check |
| 1. Al menos 2 alergólogos con dedicación no exclusiva. | Informe | EX | ☐ |
| 2. Área de observación en el área de administración de ITE o cerca de ella con capacidad de observación al paciente durante más de 4 horas. | Informe | EX | ☐ |
| 3. Área de atención urgente con todos los materiales necesarios para el tratamiento de reacciones adversas, que permita el inicio de maniobras de RCP con proximidad a la UCI, y una línea telefónica para llamar a la UCI. | Informe | EX | ☐ |
| 4. Disponibilidad del siguiente material para el diagnóstico y tratamiento de reacciones adversas: 1-Carro de reanimación completo (con desfibrilador y todos los suministros y medicamentos necesarios para responder al paro cardiorrespiratorio). 2. Monitor de constantes vitales. | Fotos | EX | ☐ |
| 5. Posibilidad de utilizar datos del registro médico de pacientes a través de ordenador accesible para todos los miembros de la unidad. | Informe | EX | ☐ |
| 6. Posibilidad de usar extractos experimentales (en investigación, no comercializados). | Informe | EX | ☐ |
| 7. Posibilidad de administrar ITE en pacientes de alto riesgo (ej. mastocitosis, reacciones sistémicas previas). | Informe | EX | ☐ |
| 8. Completar el documento de instrucciones individualizado al menos en el 90% de las veces. | Informe | EX | ☐ |
| 9. Disponibilidad de una lista de verificación para la administración de ITE de acuerdo con el nivel de pacientes que pueden ser tratados (alto riesgo) con variables específicas. | Informe y Documento | EX | ☐ |
| 10.Completar la lista de verificación en al menos el 90% de los casos | Informe | EX | ☐ |
| 11.Posibilidad de acceder a los datos de forma informática para recoger las dosis administradas. | Informe | EX | ☐ |
| 12.Monitorizar la eficacia y seguridad usando unos parámetros objetivos. | Informe | EX | ☐ |
| 13.Aplicar medidas de control de almacenamiento del extracto (termómetro) y garantizara la conservación a la temperatura correcta. | Informe | EX | ☐ |
| 14.Disponer de un plan de seguridad que incluya la monitorización. | Informe y Documento | EX | ☐ |
| 15.Disponibilidad de un cuestionario de satisfacción del paciente. | Informe y Documento | EX | ☐ |
| 16.Calendario específico para ITE que incluya huecos para consultas urgentes de los pacientes sin cita. | Informe | EX | ☐ |
| 17.Disponibilidad de documento detallado o registro con todos los datos relacionados con la ITE, que incluya información sobre el extracto, la dosis, tolerabilidad, fecha de inicio, medidas del PEF. | Informe y Documento | EX | ☐ |
| 18.Respuesta a incidencias relacionadas con ITE en 48-72 horas. | Informe | EX | ☐ |
| 19.Registro de incidentes en más del 80% de los casos. | Informe | EX | ☐ |
| 20.Acreditación de formación médica continuada en Inmunoterapia, del personal médico de la unidad de IT. | Certificados DPC Diplomas | EX | ☐ |
| 21.Formar parte como miembro en una red específica de IT o participación en algún proyecto de IT específica en los últimos 5 años. | Aval documental | EX | ☐ |
| 22.Sistema de auditoría interna para evaluar la recogida de reacciones adversas. | Informe | EX | ☐ |
| 23.Implementación del ciclo PDCA para la mejoría continuada. | Documento | EX | ☐ |
| 24.Miembros pertenecientes a sociedades científicas. | Certificados | EX | ☐ |
Una vez tenga preparada la documentación presente su solicitud en estos enlaces:
Si tiene cualquier duda o consulta, contacte a: uit@seaic.org.
Unidades de inmunoterapia acreditadas
Acreditaciones 2023: 5 Unidades de Inmunoterapia Avanzada Acreditadas
5 UNIDADES DE INMUNOTERAPIA DE AVANZADA ACREDITADAS
| CENTRO | CIUDAD | TITULAR |
|---|---|---|
| CONSORCI SANITARI ALT PENEDÈS-GARRAF | Barcelona | Dra. Catalina Gómez Galán |
| CONSORCI SANITARI DE TERRASSA | Terrassa, Barcelona | Dra. Marta Viñas Domingo |
| HOSPITAL UNIVERSITARI SANTA MARÍA | Lleida | Dr. Lluís Marquès Amat |
| HOSPITAL UNIVERSITARIO DONOSTIA, SECCIÓN ALERGIA INFANTIL | San Sebastián, Guipúzcoa | Dr. Alejandro Joral Badas |
| HOSPITAL HLA JEREZ PUERTA DEL SUR, UNIDAD DE ALERGOLOGÍA | Jerez de la Frontera, Cádiz | Dr. Antonio Letrán Camacho |
Acreditaciones 2023: 9 Unidades de Inmunoterapia de Excelencia Acreditadas
9 UNIDADES DE INMUNOTERAPIA DE EXCELENCIA ACREDITADAS
| CENTRO | CIUDAD | TITULAR |
|---|---|---|
| HOSPITAL GENERAL UNIVERSITARIO GREGORIO MARAÑÓN | Madrid | Dra. Blanca Noguerado Mellado |
| COMPLEXO HOSPITALARIO UNIVERSITARIO DE PONTEVEDRA | Pontevedra | Dra. Celsa Pérez Carral |
| HOSPITAL REINA SOFIA | Córdoba | Dra. Pilar Serrano Delgado |
| HOSPITAL UNIVERSITARIO DE CANARIAS | Santa Cruz de Tenerife | Dra. Mª Inmaculada Sánchez Machín |
| HOSPITAL UNIVERSITARIO DE FUENLABRADA | Fuenlabrada, Madrid | Dra. Eloína González Mancebo |
| HOSPITAL UNIVERSITARIO GERMANS TRIAS PUJOL | Badalona, Barcelona | Dr. Albert Roger Reig |
| HOSPITAL UNIVERSITARIO INFANTA LEONOR | Madrid | Dra. Paula López González |
| HOSPITAL UNIVERSITARIO INFANTA SOFIA | Madrid | Dra. Beatriz Núñez Acevedo |
| HOSPITAL UNIVERSITARIO LA PAZ | Madrid | Dra. Margarita Tomás Pérez |
Acreditaciones 2022: 5 Unidades de Inmunoterapia Avanzada Acreditadas
UNIDADES ADICIONALES
| CENTRO | CIUDAD | TITULAR |
|---|---|---|
| HOSPITAL UNIVERSITARIO DONOSTIA. Sección Alergia Adultos. | San Sebastián, Guipúzcoa | Dr. Alejandro Joral Badas |
| CLÍNICA DERMATOLOGIA Y ALERGIA | Badajoz | Dr. Irán Sánchez Ramos |
| HOSPITAL UNIVERSITARIO REINA SOFIA | Córdoba | Dr. Pilar Serrano Delgado |
| CEP EL ARROYO. HOSPITAL UNIVERSITARIO DE FUENLABRADA | Fuenlabrada | Dra. Eloina Gonzalez Mancebo |
| COMPLEJO ASISTENCIAL UNIVERSITARIO DE PALENCIA | Palencia | Dra. María Isabel Garcimartín Galicia |
Comisión de acreditación
| Coordinador: | Javier Sola Martínez |
| Vocales: | David El-Qutob López Eloína González Mancebo Beatriz Núñez Acevedo Albert Roger Reig Ana Tabar Purroy Marcela Valverde Monge |
Campaña web del CNPT
El Comité Nacional para la Prevención del Tabaquismo ha lanzado la campaña web para apoyar la modificación legislativa sobre el consumo de tabaco, respaldada por la SEAIC.
Descargar documento: ![]() ¿Por qué nosotros no? (3211 descargas )
¿Por qué nosotros no? (3211 descargas )
Aval SEAIC
Directorio de productos avalados por SEAIC (en orden alfabético).
Allerban
Tratamiento anti-ácaro y antibacteriano integrado en las fibras para relleno de almohadas y edredones Hollofill, Qualofill y Comforel.Allerbran es una protección anti-ácaros y antimicrobiana que impide el desarrollo de los ácaros del polvo en las fibras textiles.Su mecanismo de acción es a través de una sustancia biológica activa incorporada en la fibra textil de polipropileno o de poliéster que elimina el hongo Aspergillus repens, esencial para que el aparato digestivo de los ácaros pueda asimilar los nutrientes habituales. Se registró en la EPA en 1976 y ha sido utilizada de forma segura durante más de 20 años en otros campos (ej. Ropa interior, pañales, gasas estériles). Su eficacia contra los microorganismos es de una naturaleza mecánica pura, mediante un método mecánico de rotura de la pared celular del mismo que conlleva la destrucción de la célula.
Filvit Alergenos
Filvit Alérgenos reduce hasta 6 meses la concentración de alérgenos de ácaros domésticos. Laborotario Ern.
Plasma Quad/Plasma Quad Plus
Mitsubishi Electric, fabricante de equipos de Aire Acondicionado, dispone del exclusivo sistema de filtrado de aire Plasma Quad y, su evolución Plasma Quad Plus. Una tecnología incorporada en los splits de aire acondicionado MSZ-FH Kirigamine y MSZ-LN Kirigamine Style capaz de eliminar eficazmente las partículas contaminantes del aire.
Según los estudios realizados por la marca japonesa, los filtros Plasma Quad y Plasma Quad Plus reducen hasta el 97% la exposición a partículas alergénicas, virus y bacterias, lo que puede contribuir a controlar los síntomas de alergia.
Gracias a esta elevada efectividad en la eliminación de contaminantes del aire, los filtros Plasma Quad son la nueva opción en Aire Acondicionado de Mitsubishi para personas alérgicas y/o asmáticas interesadas en crear un ambiente saludable y libre de impurezas en su hogar.
![]() Plasma Quad/Plasma Quad Plus(5093 descargas)
Plasma Quad/Plasma Quad Plus(5093 descargas)
Seminarios web anteriores COVID-19
Tratamiento antiinflamatorio en la COVID-19. ¿Amigos o enemigos?
28 de mayo de 2020
Queremos agradecer la colaboración técnica de Astra Zeneca en la realización de esta sesión científica.
COVID-19, asma o rinitis. ¿Cómo diferenciarlos?
27 de mayo de 2020
Queremos agradecer la colaboración técnica de Menarini en la realización de esta sesión científica.
![]() Programa seminario web "COVID-19, asma o rinitis. ¿Cómo diferenciarlos?" (1658 descargas )
Programa seminario web "COVID-19, asma o rinitis. ¿Cómo diferenciarlos?" (1658 descargas )
Impacto del COVID-19 en alergia respiratoria y rinología
19 de mayo de 2020
Queremos agradecer la colaboración técnica de Uriach en la realización de esta sesión científica.
![]() Programa seminario web "Impacto del COVID-19 en alergia respiratoria y rinología" (2052 descargas )
Programa seminario web "Impacto del COVID-19 en alergia respiratoria y rinología" (2052 descargas )
COVID-19: Etiopatogenia, Clínica Nasal y Cutánea
14 de mayo de 2020
Queremos agradecer la colaboración técnica de Novartis en la realización de esta sesión científica.
![]() Programa seminario web "COVID-19: Etiopatogenia, Clínica Nasal y Cutánea" (2154 descargas )
Programa seminario web "COVID-19: Etiopatogenia, Clínica Nasal y Cutánea" (2154 descargas )
El día después en una consulta de alergología: opciones de desescalada
11 de mayo de 2020
Queremos agradecer la colaboración técnica de Diater Laboratorios en la realización de esta sesión científica.
![]() Programa Seminario Web "El Día Después en una Consulta de Alergología" (2001 descargas )
Programa Seminario Web "El Día Después en una Consulta de Alergología" (2001 descargas )
Alergia en Tiempos de Covid-19
30 de abril de 2020
Queremos agradecer la colaboración técnica de Laboratorios Leti en la realización de esta sesión científica.
![]() Programa Webinar «Alergia en Tiempos de Covid-19»
Programa Webinar «Alergia en Tiempos de Covid-19»
Alergia Respiratoria y COVID-19
16 de abril de 2020
Queremos agradecer la colaboración técnica de GSK en la realización de esta sesión científica.
![]() Programa Webinar SEAIC "Alergia Respiratoria y COVID-19" (3637 descargas )
Programa Webinar SEAIC "Alergia Respiratoria y COVID-19" (3637 descargas )
Estadísticas del portal web de la SEAIC (2010-2011)
En los dos últimos años se han registrado 190.071 visitas en el portal web de la SEAIC. Hasta el momento, el sitio comprende 173 páginas, con 182 entradas de noticias y 412 documentos para la descarga.
Protocolo Inicio Berinert Subcutáneo
El Grupo Español de Estudio del Angioedema mediado por Bradicinina (GEAB) de la SEAIC ha publicado su Protocolo de inicio de tratamiento con Berinert® subcutaneo como profilaxis a largo plazo en pacientes con Angioedema Hereditario por Déficit de C1-inhibidor (AEH-C1-INH), disponible para descarga en nuestra página web.
Seminario web alergia a himenópteros
El próximo 14 de abril, tendrá lugar el seminario web titulado «Nuevo abordaje en el tratamiento de los pacientes alérgicos a Apis y Vespula. Moving into a new phase for treatment of Bee and Wasp Allergy Immunotherapy», organizado por laboratorios ALK-Abelló y que cuenta con el aval de la SEAIC.
![]() Seminario web Alergia a himenópteros 14/04/2021 (1659 descargas )
Seminario web Alergia a himenópteros 14/04/2021 (1659 descargas )
Traslado web CYNA
El material referente a la XI Reunión CYNA, incluyendo los videos de las sesiones, se ha trasladado a la web de Desarrollo Profesional Continuado, donde se ha incluido como curso on-line.
Alergia a himenópteros
Protocolos clínicos para la alergia a los insectos himenópteros
Introducción
Las abejas, las avispas y sus picaduras forman parte de nuestro entorno y tanto el cambio climático como la polución inciden en un aumento de la posibilidad de picaduras por insectos. Hay datos que indican que el 56,6% al 94,5% de la población adulta ha sido picada al menos una vez en su vida.
Se estima que estas picaduras pueden producir una reacción local extensa en el 2,3% a 18,6% de la población, y aunque las reacciones sistémicas graves en España son poco frecuentes, con una tasa entre el 2,3% y el 2,8% de la población rural, debemos tener en cuenta que es una enfermedad potencialmente mortal.
El uso de la telemedicina para el seguimiento de la alergia a los insectos himenópteros puede servir para:
- 1 Optimizar la visita presencial a la consulta del alergólogo.
- 2 Evitar desplazamientos innecesarios en el caso de evolución favorable y posibilidad de solucionar dudas de forma diferida o a distancia.
- 3 Repasar el protocolo de actuación en el caso de picadura por insectos himenópteros esté el paciente o no con un tratamiento de inmunoterapia frente al veneno de un himenóptero.
- 4 Mejorar la comunicación profesional sanitario-paciente.
- 5 Posibilidad de realizar la primera consulta (solo anamnesis y solicitud de pruebas) de forma telemática, optimizando el tiempo y los recursos utilizados.
Este protocolo se basa en el documento elaborado por el comité de himenópteros de la SEAIC denominado: «Alergia a himenópteros: Recomendaciones y algoritmos de práctica clínica de la Sociedad Española de Alergología e Inmunología Clínica. Actualización. 2021«.
El manejo de la alergia al veneno de los himenópteros conlleva ciertas dificultades. La aparición de sensibilizaciones a varios insectos, o la negatividad de los estudios obliga a utilizar técnicas más complejas para afinar el diagnóstico. En ocasiones la tolerancia a la inmunoterapia no es óptima, y se precisan cambios en las pautas o pretratamientos que permitan continuarla durante el tiempo adecuado para obtener la protección del paciente. La falta de eficacia de la inmunoterapia en algunos pacientes supone también un reto para el alergólogo.
Además, se incluyen algunas de las recomendaciones del grupo de trabajo sobre m-health o m-salud de la Academia Europea de Alergología e Inmunología Clínica (EAACI).
Aunque las tecnologías de mHealth pueden ser muy útiles para la prevención y el tratamiento de la alergia al veneno de los himenópteros, el número de aplicaciones existentes es limitado. Se podrían utilizar aplicaciones para informar gráficamente la presencia de diferentes especies de himenópteros o especies no comunes en determinadas regiones. Los excursionistas o viajeros pueden utilizarlos para tomar fotografías de especies, que serán identificadas e informadas automáticamente. Esto puede utilizarse como base para la creación de sistemas de alerta de insectos potencialmente peligrosos. Además, la mHealth puede servir para comunicarse con servicios de Urgencias o con determinadas autoridades sanitarias en regiones particularmente aisladas o cuando no hay ayuda disponible en caso de una reacción alérgica potencialmente grave. Además, la mHealth también podría ayudar a registrar e identificar el insecto culpable después de una picadura. Por lo tanto, todas estas posibles aplicaciones podrían mejorar la identificación de pacientes alérgicos al veneno de los himenópteros y podrían contribuir a la prevención de la aparición o desarrollo de reacciones graves.
Además, se deben desarrollar aplicaciones móviles para monitorizar el curso del tratamiento de la inmunoterapia con veneno (VIT), incluidas la dosis, las reacciones locales o reacciones adversas sistémicas y la creación de recordatorios de la siguiente cita para recibir la dosis de inmunoterapia correspondiente. Se necesitan estudios para evaluar si la salud móvil también puede mejorar la adhesión a la VIT y hacer que los pacientes sean corresponsables de su propio tratamiento, así como aumentar la consciencia sobre la importancia y la idoneidad de la inmunoterapia con veneno de himenópteros.
Con relación a la anafilaxia, la EAACI indica que las herramientas de mHealth que se utilizan actualmente tienen fines educativos e intervencionistas. Los materiales educativos pueden aumentar el conocimiento entre los grupos objetivo, pero también entre otros individuos como maestros, enfermeras, personal preescolar y familiares u otras personas que puedan necesitar actuar durante una reacción anafiláctica. El reconocimiento de los síntomas clave se puede apoyar ofreciendo ejemplos visuales (fotografías, vídeos). El rendimiento de las medidas de tratamiento agudo, especialmente la aplicación de un autoinyector de epinefrina (AAI), se puede mejorar mediante planes de acción para la anafilaxia administrados a través de tecnologías de salud móvil. Este soporte puede implementarse a través de instrucciones de audio directas o llamadas de emergencia automatizadas. Actualmente se están desarrollando nuevos sistemas de alerta para identificar a los portadores de autoinyectores de epinefrina y los departamentos de emergencia cercanos. Ya se han utilizado con éxito alertas automáticas que indican al paciente la caducidad de su autoinyector de epinefrina. Como la anafilaxia pone en peligro la vida pero es poco común, el desarrollo y la implementación de herramientas de capacitación móviles es de alta prioridad para facilitar la capacitación repetida y así optimizar la competencia de los pacientes, médicos y otras personas involucradas. Hay una gran cantidad de materiales disponibles. Un ensayo clínico reciente sobre el uso de un estuche inteligente para autoinyectores de epinefrina mostró una mayor satisfacción relacionada con una disminución de la ansiedad entre los pacientes que usaban el dispositivo. Además, los participantes informaron sobre una mejor adherencia al transporte del inyector y mejor participación en el manejo de la anafilaxia. A pesar de estos resultados prometedores, las investigaciones futuras deben incluir ensayos clínicos prospectivos que evalúen la mejora del resultado clínico de los pacientes anafilácticos en el contexto de las herramientas de salud móviles.
Seguimiento de la alergia a los insectos himenópteros
Requisitos
- Diagnóstico anterior de hipersensibilidad a uno a o varios insectos himenópteros mediante visita presencial con especialista.
- Disposición de teléfono o Internet.
- No sufrir ninguna discapacidad que impida usar ninguno de estos sistemas.
- El paciente menor de <18 años debe estar acompañado por un progenitor o persona responsable.
- Consentimiento verbal o escrito del paciente o tutor legal, que debe reflejarse en la historia clínica. Actualmente la normativa no exige el consentimiento por escrito.
Fase de preparación
Envío de correo electrónico o mensaje de texto en aplicación segura al menos 1 semana antes con:
- Fecha y hora de la visita.
- Cuestionario de Calidad de vida en alérgicos a veneno de himenópteros (HiCAVi), con instrucciones de su cumplimentación el mismo día de la consulta.
- Instrucciones para disponer en el momento de la consulta del cuestionario HiCAVi ya cumplimentado, su autoinyector de epinefrina, y el plan de acción en el caso de picadura por un insecto himenóptero
- Valoración de pruebas complementarias, si estas han sido solicitadas en la visita presencial anterior.
Esta fase puede estar dirigida a una visita de revisión ya programada o a una visita solicitada por el propio paciente para resolver dudas o abordar una nueva reacción por picadura de insecto himenóptero
El departamento de alergia deberá disponer de un servicio de mensajería segura para que el paciente pueda solicitar una visita en cualquier momento.
Consulta telemática
Se realiza mediante llamada telefónica o plataforma para videoconsultas. Se aconseja realizar consultas síncronas aunque la disposición de consultas asíncronas puede ayudar a mejorar la accesibilidad del sistema y su usabilidad para el paciente. Comenzar siempre la consulta telemática presentándonos. Durante el su desarrollo de la consulta se abordarán los siguientes aspectos:
Anamnesis se evalúan:
- Historia clínica: anamnesis y posible Identificación del insecto.
- 1 Diferenciar Tipo de Reacción: Local/Local Extensa/Sistémica (Grados I-IV de Muller y 1-3 de EAACI).
- 2 Tipo de insecto (idenficarlo, si es posible): ¿Avispa/Abeja/Otro?
- 3 Estación del año y entorno donde sucedió la picadura (rural, urbano, comida, piscina, deporte, etc.).
- 4 Número de picaduras.
- 5 Sitio de picadura en el cuerpo.
- 6 Sitio de picadura en el cuerpo.
- 7 Intervalo de tiempo entre la picadura y el inicio de síntomas.
- 8 Tipo de síntomas presentados.
- 9 Tratamiento administrado.
- 10 Algoritmo REMA*
- 11 Riesgo de nuevas reacciones:
- Frecuencia de exposición a himenópteros.
- Tipo de reacción previa sufrida.
- Factores que se asocian a la mayor gravedad.
- 1 En relación con el paciente: picadura de avispa, sexo masculino, edad > 40 años, mastocitosis o síndrome de activación mastocitaria clonal, triptasa sérica elevada y déficit de PAF-acetilhidrolasa.
- 2 Con relación a picadura previa: intervalo rápido entre picadura e inicio de síntomas y ausencia de síntomas cutáneos.
- Con relación al tratamiento: retardo en el uso de epinefrina y mantener al sujeto en bipedestación.
Solicitud de pruebas de forma diferida:
Si reacción generalizada con la picadura de un himenóptero y en algunos pacientes con reacciones locales extensas, con alta exposición y/o mala calidad de vida, con vistas a valorar la indicación de inmunoterapia.
No está indicado el estudio predictivo en pacientes con miedo a reacciones, o con familiares alérgicos, ya que es frecuente la positividad de pruebas cutáneas y/o IgE específica en sangre en personas no alérgicas.
- 12 Triptasa.
- 13 Pruebas cutáneas.
- 14 IgE total e IgE específica venenos.
Adhesión terapéutica: En el caso de VIT, si está recibiendo la inmunoterapia:
- Lugar de administración: Hospitalaria/Extrahospitalaria.
- Frecuencia:
- Dosis iniciales: semanales
- Dosis mantenimiento: mensuales, bimensuales, otra frecuencia.
Técnica de uso de autoinyector de epinefrina: Visualización de la técnica de uso del autoinyector de epinefrina de paciente (o la persona responsable) y corrección de errores detectados. Exige el uso de plataforma de videoconsulta. Mostrar vídeos o realización por parte de profesional sanitario.
Tratamiento con fármaco biológico en pacientes con mala tolerancia a vacuna (si pertinente): Interrogar sobre posibles efectos adversos inmediatos y tardíos, cumplimiento de las dosis, deseo de administración hospitalaria o domiciliaria y registro de número de dosis administradas desde inicio o última revisión. La disposición de sistemas de recordatorios a los pacientes con las fechas recomendadas de administración puede mejorar la adhesión.
Tratamiento con inmunoterapia específica (si pertinente): Interrogar sobre posibles reacciones inmediatas y tardías (locales y sistémicas), cumplimiento de las dosis, administración en centro médico y registro de número de dosis administradas desde inicio o última revisión. La disposición de sistemas de recordatorios a los pacientes con las fechas recomendadas de administración puede mejorar la adhesión.
Factores agravantes potenciales: Interrogatorio sobre posibles cofactores exacerbantes de reacción adversa a inmunoterapia frente a veneno de himenópteros o de una anafilaxia en el caso de picadura de insectos.
Programación de la siguiente visita: Programar la próxima cita en función del resultado de la consulta actual, si se ha realizado pruebas previamente o si se las tuviera que realizar:
1ª consulta: En pacientes que la 1ª consulta ha sido la inicial, realizar pruebas cutáneas y analítica para ser evaluadas bien presencialmente o bien telemática en el plazo de 1 mes después de la 1ª visita.
Consultas sucesivas: En el caso de recibir VIT: 1 consulta anual telemática, valorando los mismos aspectos que en la primera consulta.
- Dentro de esta programación pueden solicitarse pruebas complementarias si se considera necesario y que el paciente podrá aportar en una próxima consulta telemática o presencial. Asegurar al menos una visitas presenciales anual.
- Tras un ingreso hospitalario o visita a urgencias por una anafilaxia secundaria a picadura de insecto es recomendable una consulta telemática dentro de los primeros 30 días, dependiendo del contexto clínico y social.
La consulta remota debe quedar siempre reflejada en la historia clínica del paciente. Finalizar siempre la consulta preguntando si queda alguna pregunta por responder.
Consultas asíncronas: Aunque se aconseja realizar consultas síncronas, la disposición de consultas asíncronas puede ayudar a mejorar la accesibilidad del sistema y su usabilidad para el paciente. En caso de optar por esta modalidad debe disponerse siempre de un correo electrónico seguro con dirección de correo electrónico corporativa. A través de esta vía pueden enviarse al paciente:
- Cuestionario HiCAVi
- Informes clínicos actualizados.
- Planes de tratamiento nuevos.
- Aplicaciones recomendadas.
- Copias de analíticas del paciente.
Algoritmo REMA:
- Sexo: Hombre +1; Mujer -1
- Síntomas clínicos:
- Ausencia de urticaria o angioedema +1
- Urticaria y/o angioedema -2
- Presíncope y/o síncope +3
- Presíncope y/o síncope +3
- < 15 ng/mL -1
- ≥ 25 ng/mL +2
- Puntuación < 2: Baja probabilidad de SAMc
- Puntuación > 2: Alta probabilidad de SAMc
Sensibilidad: 0,92; Especificidad: 0,81; Valor predictivo positivo: 0,89; Valor predictivo negativo: 0,87.
Aplicaciones y páginas web de apoyo a la consulta telemática de alergia al veneno de los himenópteros
Documento de recomendaciones y algoritmo: Alergia a himenópteros: Recomendaciones y algoritmos de práctica clínica de la Sociedad Española de Alergología e Inmunología Clínica. Actualización. 2021.
Matricardi PM, Dramburg S, Alvarez-Perea A, Antolín-Amérigo D, Apfelbacher C, Atanaskovic-Markovic M, et al. The role of mobile health technologies in allergy care: An EAACI position paper. Allergy. 2020 Feb;75(2):259-272. doi: 10.1111/all.13953. Epub 2019 Sep 16. PMID: 31230373.
Hernandez‐Munoz LU, Woolley SI, Luyt D, et al. Evaluation of al ‐lergisense smartphone tools for adrenaline injection training.IEEE J Biomed Health Inform. 2017;21:272‐282.
Fernandez‐Mendez F, Saez‐Gallego NM, Barcala‐Furelos R, et al. Learning and treatment of anaphylaxis by laypeople: a simulation study using pupilar technology.Biomed Res Int. 2017;2017:9837508.
Cardona V, Luengo O, Labrador‐Horrillo M, et al. First clinical trial with a medical device for anaphylaxis management. J Allergy Clin Immunol. 2018;2:141. Supplement, page AB149.
Sala-Cunill A, Luengo O, Curran A, Moreno N, Labrador-Horrillo M, Guilarte M, Gonzalez-Medina M, Galvan-Blasco P, Cardona V. Digital technology for anaphylaxis management impact on patient behaviour: A randomized clinical trial. Allergy. 2021 May;76(5):1507-1516. doi: 10.1111/all.14626. Epub 2020 Nov 4. PMID: 33043475.